Atomistica 2016
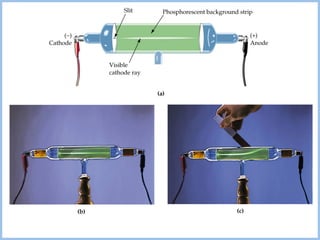
- 3. Prof. Júlio Xavier e a massa da bola, poderemos prever qual o desvio que ela irá sofrer. Por exemplo, uma bola de golfe desviará muito menos que uma bola de pingue-pongue, devido à diferença entre suas massas. Portanto, o desvio permitirá calcular a massa. + – – cátodo ânodo feixe de elétrons tela fluorescente ação do campo elétrico E e do campo magnético B Experimento: Raios catódicos sob a ação de um campo elétrico. Com os raios catódicos, é um pouco mais complicado do que com bolas de golfe, porque o efeito do vento é substituído por um campo elétrico e um campo magnético, que agem sobre o elétron carregado negativamente. O desvio produzido é proporcional à carga do elétron e inversamente proporcional a sua massa. Visto que esse tipo de medida dá apenas uma resposta, encontramos na experiência de Thomson somente o valor da relação carga / massa.
- 4. Pudim de Passas Prof. Júlio Xavier “Plum Pudding”: Pudim de passas ou de ameixas
- 5. Prof. Júlio Xavier O modelo atômico de Thomson explicava satisfatoriamente os seguintes fenômenos: • eletrização por atrito; • corrente elétrica; • formação de íons; • descargas elétricas em gases;
- 7. Reproduçãoproibida.Art.184doCó Acompanhando a figura acima, vemos ão que um pedaço do metal polônio emi- m feixe de partículas a, que atravessa uma na finíssima de ouro. Rutherford obser- então, que a maior parte das partículas ravessava a lâmina de ouro como se esta e uma peneira; apenas algumas partícu- desviavam ou até mesmo retrocediam. Como explicar esse fato? Polônio Feixe de partículas a Bloco de chumbo Placa de chumbo com um orifício central Lâmina finíssima de ouro Papel fotográfico Impressões ou manchas fotográficas Ernest Rutherford Nasceu em Nelson (Nova Zelândia), em 1871. Foi professor no Canadá e na Inglaterra — nas universidades de Manchester e Cambridge. Trabalhou com ondas eletromagnéticas, raios X, radioatividade e teoria nuclear, e reali- zou a primeira transmutação artificial. Recebeu o Prêmio Nobel de Química em 1908. Faleceu em 1937. Em sua ho- menagem, o elemento químico 104 foi chamado de rutherfórdio (Rf). GARCIA-PELAYO/CID LEM 29/5/05, 18:2978 erford viu-se obrigado a admitir que a lâmina de ouro não era constituída de átomos justapostos, como pensaram Dalton e Thomson. Ao contrário, ela seria formada por equenos, densos e positivos, dispersos em grandes espaços vazios, como esquematizados andes espaços vazios explicam por que a grande maioria das partículas a não sofre desvios. Partícula que retrocedeu Partícula desviada Feixe de partículas a Partículas com percurso inalterado Partícula que retrocedeu Átomos da lâmina de ouro Partícula desviada
- 8. Prof. Júlio Xaviercaso de uma partícula a; no caso extremo de + – – – – – Modelo planetário
- 9. Prof. Júlio Xavier denominados átomos. Um átomo é um conjunto formado por um certo número de prótons e nêutrons, constituindo um núcleo, ao redor do qual gira um número de elétrons igual ao número de prótons, que constitui a eletrosfera. Partículas Região (localização) Carga elétrica Massa absoluta / g Massa relativa Prótons Núcleo +1 1,672x10–24 1 Nêutrons Núcleo 0 1,675x10–24 1 Elétrons Eletrosfera –1 9,109x10–28 1 1 836 OBSERVAÇÃO Partículas subatômicas
- 10. Prof. Júlio Xavier – – – – – Núcleo Formado por prótons e nêutrons Eletrosfera Formada por elétrons distribuídos em várias camadas es menor que a de um próton ou de um Composição fundamental dos átomos: Concentração das massas
- 11. Prof. Júlio Xavier A identificação dos átomos com número atômico 11. Outros exemplos: mero atômico 17 identifica os átomos de cloro; mero atômico 26 identifica os átomos de ferro; etc. ão geral de um átomo é: mplo: 35 17Cl ou 17Cl35 indica um átomo de cloro que possui 17 prótons e 18 número de massa é, pois 17 1 18 5 35. Z A X ou ZXA Número de massa Número atômico 6/7/05, 14:2882
- 12. Prof. Júlio Xavier Semelhanças atômicas: isoátomos Espécies químicas que apresentam o número atômico (Z), o número de nêutrons (N) ou o número de massa (A) iguais. Isotopos
- 13. Prof. Júlio Xavier Semelhanças atômicas Isobaros são átomos de diferentes números de prótons mas que possuem o mesmo número de massa Isotonos são átomos de diferentes números de prótons, diferentes números de massa, porém com mesmo número de nêutrons.
- 14. Prof. Júlio Xavier Íons: mente neutro, ou seja, o número de elétrons na , e em conseqüência suas cargas se anulam. étrons da eletrosfera, sem sofrer alterações em seu . rna m- êu- ns- ns, um o: o 11 on ns. seu nui ca- vel. -dia. Um perfeito equilíbrio entre os íons Na1 e K1 , das células de nosso organismo. Ao colocarmos sal verdade colocando íons Na1 e Cl2 . ro de nêutrons (N) e o número de massa (A) de e átomos com um ou outro número igual. A partir Cl0 Cl– – Átomo de cloro (eletricamente neutro) Ânion cloreto (tem uma carga negativa) Átomo de sódio (eletricamente neutro) Cátion sódio (tem uma carga positiva) – Na0 Na+ (Esquemas com uso de cores-fantasia; sem escala) n negativo, também chamado ânion. Por exem- átomo normal de cloro tem 17 prótons, 18 nêu- 17 elétrons. Ele pode ganhar 1 elétron e trans- -se em ânion cloreto (Cl2 ), que terá 17 prótons, trons e 18 elétrons. uando um átomo perde elétrons, ele se torna um sitivo, também chamado cátion. Por exemplo: o de sódio (Na) tem 11 prótons, 12 nêutrons e 11 ns.Elepodeperder1elétron, tornando-seumcátion Na1 ) com 11 prótons, 12 nêutrons e 10 elétrons. bserve que, quando um átomo ganha elétrons, seu ho aumenta; quando ele perde elétrons, diminui anho; mas em ambos os casos sua massa pratica- não se altera, pois a massa do elétron é desprezível. s íons estão sempre presentes em nosso dia-a-dia. Um perfeito equilíbrio entre os íons Na1 e K1 , emplo, é fundamental para o funcionamento das células de nosso organismo. Ao colocarmos sal o de sódio) em nossos alimentos, estamos na verdade colocando íons Na1 e Cl2 . sótopos, isóbaros e isótonos aminando o número atômico (Z), o número de nêutrons (N) e o número de massa (A) de tes átomos, podemos encontrar conjuntos de átomos com um ou outro número igual. A partir giram alguns novos conceitos que agora passamos a definir: Isótopos são átomos com mesmo número de prótons (Z ) e diferente número de massa (A). Cl0 Cl– – Átomo de cloro (eletricamente neutro) Ânion cloreto (tem uma carga negativa) Átomo de sódio (eletricamente neutro) Cátion sódio (tem uma carga positiva) – Na0 Na+ NH4Cl
- 15. Prof. Júlio Xavier Semelhanças atômicas Isoletrônicos
- 16. Prof. Júlio Xavier A ilustração acima mostra um espectro contínuo, pois as cores vão variando gradativamente do vermelho ao violeta — que são os dois limites extremos para nossa visão. Fenômeno idêntico ocorre na formação do arco-íris, em que as gotículas de água no ar agem sobre a luz do mesmo modo que o prisma de vidro. Em nosso cotidiano, o exemplo mais comum de onda ou oscilação eletromagnética é a luz. Uma observação de grande importância é notar o comportamento da luz ao atravessar um prisma de vidro. Um feixe de luz branca (luz solar ou de uma lâmpada incandescente comum) se decompõe em várias cores, que formam o chamado espectro luminoso, conforme mostramos na ilustração a seguir: Vista frontal do anteparo Vermelho Alaranjado Amarelo Verde Azul Anil Violeta Anteparo Prisma Lâmpada incandescente Dispersão da luz branca através de um prisma. J.GUTIIERREZSANCHEZ/CID
- 17. Prof. Júlio Xavier um tubo semelhante ao de Geissler (página 75), contendo o gás hidrogênio a ba tensão elétrica (“lâmpada” de hidrogênio), o fenômeno observado seria bem dif gar do espectro contínuo (isto é, contendo todas as cores), vemos agora no antep nhas coloridas, permanecendo o restante totalmente escuro. Dizemos então que uo e chamamos as linhas luminosas de raias ou bandas do espectro. continuidade do espectro não ocorre só com o hidrogênio, mas com todos os eleme bém muito importante notar que as raias do espectro são constantes para um dad Vista frontal do anteparo Vermelho Azul Anil Violeta Anteparo Prisma “Lâmpada” de hidrogênio + –
- 18. Prof. Júlio Xavier A descontinuidade do espectro não ocorre só com o hidrogênio, mas com todos os elementos qu É também muito importante notar que as raias do espectro são constantes para um dado elem mico, mas mudam de um elemento para outro, como mostramos no esquema abaixo: Pois bem, no início do século XX surgiu a seguinte pergunta: estariam essas raias do espe ontínuo ligadas à estrutura atômica? É o que esclareceremos no item seguinte. . O modelo de Rutherford-Bohr O cientista dinamarquês Niels Bohr aprimorou, em 1913, o modelo atômico de Rutherford, Espectro de hidrogênio Espectro de hélio Espectro contínuo Espectro de sódio Vermelho Alaranjado VerdeAmarelo Azul Anil Violeta Comprimento de onda crescente Alguns espectros da luz visível. Cada elemento químico tem seu espectro característico, como se fosse uma “impressão digital”.
- 19. las a não sofre desvios. o caso de uma partícula da; no caso extremo de . + – – – – – Representação esquemática do modelo atômico de Rutherford. Prof. Júlio Xavier As “falhas” de Rutherford nto de rotação dos elétrons em tor- riando outro paradoxo. De fato, diz la elétrica em movimento circular stá constantemente emitindo ener- ndo (perdendo) energia, sua veloci- eo teria de diminuir com o tempo. do de encontro ao núcleo, descre- Como sair então desse impasse? É o tes. para mostrar, mais uma vez, de que maneira a ciência evolui — aos es apontadas por novas observações e experiências, sempre em bus- Núcleo Elétron –
- 20. No início do século XX... Max Planck Albert Einstein ... foi demonstrado que a energia é “quantizada”, sendo enviada em “pacotes” de ondas carregadas pelos fótons. Prof. Júlio Xavier
- 21. Prof. Júlio Xavier ; por esse motivo, as camadas são também denominad ia. Além disso, cada camada comporta um número máxim ema a seguir: 2 8 18 32 32 18 2 M N O P Q K L elétrons aumento da energia
- 22. Prof. Júlio Xavier do exterior, o xterna; a quan- m quantum de Energia rna para outra a forma de luz como ultravio- se quantum de Fóton Estado Fundamental ou estacionário energia Estado excitado
- 23. Prof. Júlio Xavier a z - e o o inidas, é fácil entender por que também bem definidas. Mais energia luminosa. Fóton Radiação eletromagnética mas dúvidas servem para mostrar, mais uma vez, de que maneira a ciência evolu ntando as contradições apontadas por novas observações e experiências, sempre s mais satisfatórios. eve estudo das ondas o para os impasses apontados no item anterior começou a surgir com a m Vamos então fazer um pequeno estudo das ondas. O exemplo mais simples : l 1 minuto Ancoradouro Observador 1 Sentido de deslocamento das ondas 234 1 2 3 4 567 8 9 10 11 12
- 24. Prof. Júlio Xavier Hoje sabemos também que o espectro completo das ondas eletromagnéticas é muito mais amplo do que o da luz visível, isto é, das ondas que podemos perceber por meio da visão. O esquema seguinte procura dar uma idéia do espectro eletromagnético completo: A velocidade de propagação (v) de todas as ondas eletromagnéticas no vácuo é igual e constante, A luz branca visível é formada por: 4 • 10 –7 l (m)5 • 10 –7 6 • 10 –7 7 • 10 –7 O espectro visível Energia solar Produzido por osciladores elétricos de corrente alternada Produzidos em reações nucleares Ultravioleta Raios cósmicos Raios g Raios X Infravermelhos Microondas e radar Rádio e TV Rádio (ondas longas) Luz visível 10 –16 10 –14 10 –12 10 –10 10 –8 10 –6 10 –4 10 –2 10 0 10 2 10 4 10 6 102 104 106 108 1010 1012 1014 1016 1018 1020 1022 1024 l (m) Hz Comprimento de onda aumenta Diâmetro do átomo Freqüência (e energia) aumenta 1 m 1 km
- 25. Prof. Júlio Xavier descontínuos aparecem sempre as mesmas raias de cores também bem de mos a ligação entre matéria e energia — nesse caso, a energia luminosa. articular do átomo de hidrogênio, temos um esquema com a seguinte rela ons e as respectivas raias do espectro: + 1 2 3 4 – – – hando a figura anterior, verifique que: quan- Três possíveis saltos do elétron do elemento hidrogênio
- 26. Prof. Júlio Xavier ro, como vimos na página 88. Se em vez da luz solar ou de uma lâmpada inca um tubo semelhante ao de Geissler (página 75), contendo o gás hidrogênio a bai tensão elétrica (“lâmpada” de hidrogênio), o fenômeno observado seria bem dife gar do espectro contínuo (isto é, contendo todas as cores), vemos agora no antep nhas coloridas, permanecendo o restante totalmente escuro. Dizemos então que o uo e chamamos as linhas luminosas de raias ou bandas do espectro. continuidade do espectro não ocorre só com o hidrogênio, mas com todos os elemen bém muito importante notar que as raias do espectro são constantes para um dado Vista frontal do anteparo Vermelho Azul Anil Violeta Anteparo Prisma “Lâmpada” de hidrogênio + –
- 27. Prof. Júlio Xavier Reproduçãoproibida.Art.184doCódigoPenaleLei9.610de19defevereirode1998. ontínuo, pois as cores vão variando gradativamente do mum de onda ou oscilação eletromagnética é a luz. Uma omportamento da luz ao atravessar um prisma de vidro. âmpada incandescente comum) se decompõe em várias noso, conforme mostramos na ilustração a seguir: Vista frontal do anteparo Vermelho Alaranjado Amarelo Verde Azul Anil Violeta Anteparo Prisma Lâmpada incandescente Dispersão da luz branca através de um prisma. cima mostra um espectro contínuo, pois as cores vão variando gradativament a — que são os dois limites extremos para nossa visão. Fenômeno idêntico ocorr -íris, em que as gotículas de água no ar agem sobre a luz do mesmo modo q Vista frontal do anteparo Vermelho Alaranjado Amarelo Verde Azul Anil Violeta Prisma Dispersão da luz branca através de um prisma. EDIA/ PRESS HOS
- 29. Prof. Júlio Xavier sódio emitem uma luz amarela quando submetidos a u verificou que diferentes elementos, submetidos a uma Elementos diferentes produzem luz com cores diferentes. A pr to Na (sódio) Sr (estrôncio)K (potássio) Cu (cobre) CEDOC
- 30. Prof. Júlio Xavier Luminosos Os letreiros luminosos, muito usados em publicidade, utilizam principalmente gás neônio (Ne) e, por isso, são conhecidos por luminosos de neon. O funcionamento desses luminosos é semelhante ao de uma lâmpada fluorescente, ou seja, os elétrons são excitados e, na sua volta à órbita original, emitem luz. As diferentes cores e tonalidades que podem ser obti- das dependem da diferença de potencial, da pressão do gás e de sua composição. e– e– e– Ne puro luz vermelha Ne + mercúrio (Hg) luz azul Ne + gás carbônico (CO2) luz violeta
