Slide apresentação sobre química II.pptx
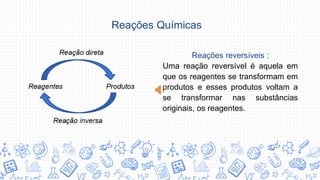
- 1. Reações Químicas Reações reversíveis : Uma reação reversível é aquela em que os reagentes se transformam em produtos e esses produtos voltam a se transformar nas substâncias originais, os reagentes.
- 2. Equilíbrio : Quando as taxas de produtos e reagentes se igualam então a reação entra em equilíbrio. Equilíbrio envolvendo íons : Equilíbrio iônico Autoionização da água : H2O(l) + H2O(l) ⮀ H3O+(aq) + OH-(aq)
- 4. Equilíbrios iônicos em solução aquosa HIDRÓLISE SALINA O conceito de hidrólise salina. Constante de hidrólise. SOLUBILIDADE DE GASES EM LÍQUIDOS Efeito da temperatura. Lei de henry Efeito da pressão. Tito e Canto volume 2. QUÍMICA na abordagem do cotidiano .
- 5. Como ocorre uma reação ? Para que uma reação química ocorra as ligações entre os átomos e moléculas devem ser rompidas e estabelecidas de outras maneiras. + → 2 moléculas 2 moléculas 2 moléculas de H2O de H2 de O2
- 6. Hidrólise salina é o nome do processo em que o cátion e/ou ânion proveniente(s) de um sal reage(m) com a água. Apenas cátions de base fraca e ânions de ácido fraco sofrem hidrólise apreciável. Reação de Neutralização ÁCIDO + BASE ⮀ SAL + ÁGUA Ex: NaOH + HCl ⮀ NaCl + H2O Como isso se aplica a Hidrólise salina?
- 7. reação de Hidrólise salina do Cianeto de Sódio H2O ⮀ H+ + OH- NaCN ⮀ Na+ + CN- O cianeto, Aniôn do ácido fraco (HCN) vai reagir com o íon H+ da água após a autoionização. Então, o processo pode ser esquematizado como : CN- + HOH ⮀ HCN + OH- Exemplificando
- 8. “A hidrólise salina altera o pH do meio, ou seja, adquire caráter ácido, básico, ou neutro”. Mas, como podemos determinar esse pH? • Solução de sal de ácido fraco e base forte é básica • Solução de sal de ácido forte e base fraca é ácida • Solução de sal de ácido forte e base forte é neutra
- 9. Sal Adquirindo caráter ácido ou básico : A) NH4Cl HCl + NH4OH NH+ 4 (aq) + H2O(l) ⮀ NH4OH(aq) + H+ B) NaHCO3 H2CO3 + NaOH HCO- 3(aq) + H2O(l) ⮀ H2CO3(aq) + OH- OH - H H - OH Hidrólise ácida Hidrólise básica
- 10. ✘
- 12. Ex. Hidrólise do NaCN, onde o CN- + HOH ⮀ HCN + OH- HCN ⮀ [ H+] [ CN-] ✘ ✘
- 13. Essas fórmulas ajudam a explicar quantitativamente por que só íon de ácido fraco ou base fraca sofre hidrólise. Quanto mais fraco for o ácido, menor será o valor de Ka . Pela fórmula, quanto menor for Ka, maior será Kh e, portanto, mais intensa será a hidrólise. Constante de hidrólise ✘
- 14. FATORES QUE ALTERAM A SOLUBILIDADE DE GASES EM LÍQUIDOS É muito difícil generalizar o comportamento da dissolução de gases em água como função da temperatura. Podemos dizer, contudo, que por via de regra ocorre uma diminuição da quantidade máxima do gás que se dissolve em água quando a temperatura aumenta, ou seja: ↑ Temperatura x Solubilidade ↓
- 15. Pressão - Lei de Henry A quantidade do gás que se dissolve em um líquido, à temperatura constante, é proporcional à pressão do gás. Caso o gás reaja com a água, isso provocará um deslocamento do equilíbrio da reação entre ambos.
- 16. ⮚ Equilíbrio entre CO2 e H2O Na figura (A) , parte do dióxido de carbono (CO2 ) presente está na fase gasosa e parte na fase aquosa. O CO2 dissolvido toma parte do equilíbrio: CO2 (aq) + H2O(l) → H+ (aq) + HCO- 3(aq) O aumento de pressão, obriga uma maior quantidade de CO2 a entrar na água. Isso desloca o equilíbrio no sentido de formação de H+. ⮚ Equilíbrio entre NH3 e H2O O equilíbrio químico estabelecido entre a amônia e a água seria: NH3 (aq) + H2O(l) → NH+ 4 (aq) + OH- (aq) Um aumento da pressão, faria uma maior quantidade de amônia se dissolver e provocaria deslocamento do equilíbrio no sentido da formação de OH-.
- 17. Oque são as “bolhas” presentes nos refrigerantes ? Ao aliviar a pressão do gás pela abertura da tampa, menos gás conseguirá ficar dissolvido, o líquido “expulsa” esse gás (CO2), daí o aparecimento imediato das borbulhas no refrigerante. • Lembre-se da Lei de Henry: “Quanto maior a pressão, maior é a quantidade de gás que se dissolve”.
- 18. Questões para fixação Questão 40. (pág 259 ) O cloreto de amônio é um sal empregado, sob orientação médica, para promover a acidificação do tubo digestivo. a) Dê a fórmula do cloreto de amônio b) Como se explica que esse sal produza solução ácida Questão 48. (pág 263) Considere o sistema que está ilustrado esquematicamente abaixo. Explique por que um aumento da pressão sobre o êmbolo faz com que ocorra um aumento do pH da solução aquosa. Sistema aquoso, contendo NH3(g) e NH3(aq) dissolvido em água
- 19. Quiz : Equilíbrios iônicos em solução aquosa Temas abordados : • Hidrólise salina. • Solubilidade de gases em líquidos. Link do quiz e código de acesso disponibilizados no Google Classroom Obs: Cadastro ou login na plataforma Quizizz (via facebook ou usando alguma conta google) ao responderem o Quiz, porfavor, coloquem o nome de vocês para que eu possa acompanhar o resultado.
- 20. OBRIGADO! Alguma dúvida? Entre em contato comigo: (88) 98132-9747 paulo.sergio.rodrigues08@aluno.ifce.edu.br