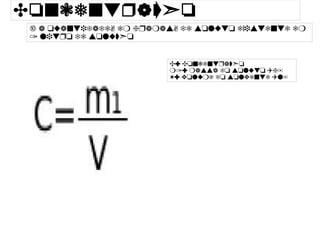
O documento apresenta as principais fórmulas relacionadas a soluções químicas, incluindo concentração, densidade, título em massa, porcentagem, molaridade, molalidade, mistura de soluções e fração molar. As fórmulas são explicadas com suas variáveis e unidades correspondentes.