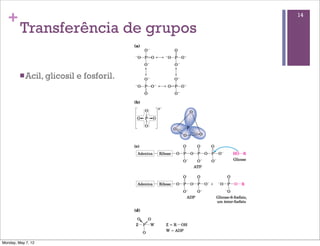
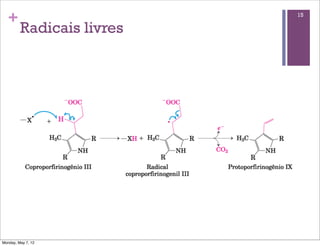
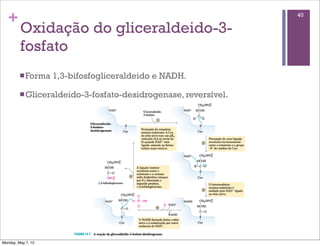
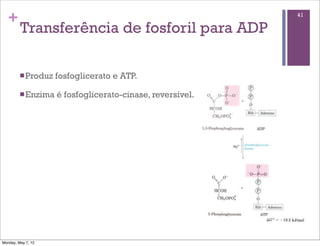
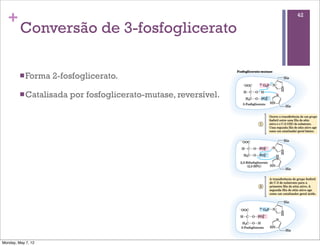
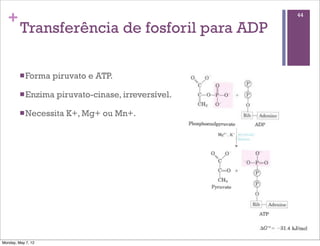
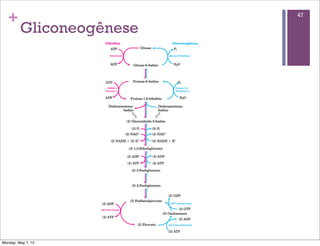
1) O documento discute os principais tópicos sobre o metabolismo, incluindo a glicólise, fermentação, destinos do piruvato, reações bioquímicas comuns e transferência de fosforil e ATP.
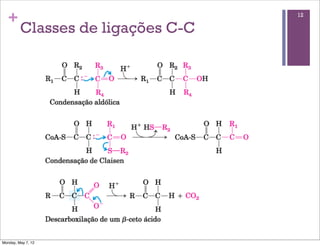
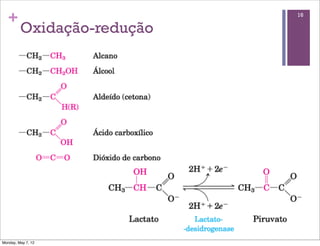
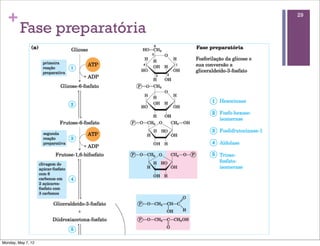
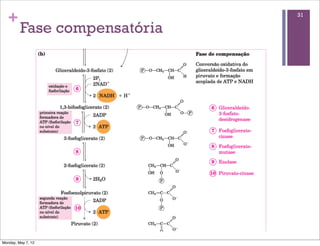
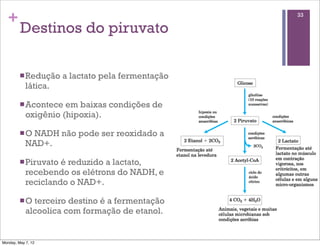
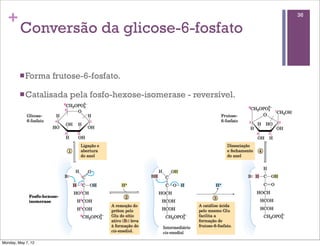
2) É explicado que a glicólise degrada a glicose em piruvato, gerando ATP e NADH, e o piruvato pode ser oxidado na mitocôndria ou reduzido a lactato.
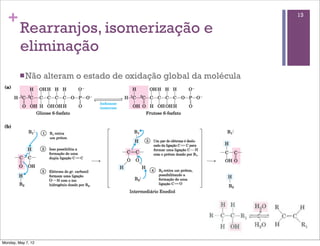
3) A regulação do metabolismo e a importância da cooperação entre sistemas enzimáticos também





![+ 8
Bioenergética e termodinâmica
n Células realizam trabalho constante.
n Precisam
de energia para manter estruturas, sintetizar
componentes, gerar corrente elétrica...
n Bioenergética => estudo quantitativo das relações de energia.
n Duas forças influenciam as reações químicas:
n Entalpia (H) - tendência de atingir o estado de ligação mais estável.
n Entropia (S) - tendência de atingir o mais alto grau de desordem.
n ∆G = ∆H - T∆S
n ∆G’o é a energia livre padrão. E a ∆G = ∆G’o + RT
ln([produtos]/[reagentes])
Monday, May 7, 12](https://image.slidesharecdn.com/gabriel-bioquimica-aula6-130317194340-phpapp02/85/Bioquimica-Aula-6-8-320.jpg)