Cálculo do calor trocado por dois mols de gás monoatômico em processo termodinâmico
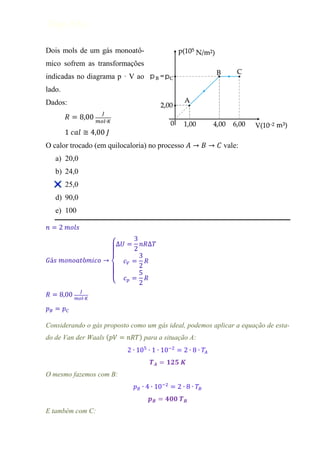
- 1. Diego Arley Dois mols de um gás monoatô- mico sofrem as transformações indicadas no diagrama p · V ao lado. Dados: O calor trocado (em quilocaloria) no processo vale: a) 20,0 b) 24,0 c) 25,0 d) 90,0 e) 100 𝑛 2 𝑚𝑜𝑙𝑠 3 ∆𝑈 𝑛𝑅∆𝑇 2 3 𝐺á𝑠 𝑚𝑜𝑛𝑜𝑎𝑡ô𝑚𝑖𝑐𝑜 𝑐𝑉 𝑅 2 5 𝑐𝑝 𝑅 2 𝐽 𝑅 𝑚𝑜𝑙 𝐾 𝑝𝐵 𝑝𝐶 Considerando o gás proposto como um gás ideal, podemos aplicar a equação de esta- do de Van der Waals ( ) para a situação A: 2 2 O mesmo fazemos com B: 2 E também com C:
- 2. Diego Arley 2 A partir do eixo das ordenadas do gráfico, temos que: 3 Para a transformação e admitindo , já que em momento algum é in- formado que a massa/quantidade de matéria do gás é mudada, temos: 2 25 25 3 ∆ ∆ 2 3 ∆ 2 ∆ 2 ∆ ∆ Analogamente: 3 ∆ 2 ∆ 2 ∆ ∆ Como a curva da transformação é uma reta, podemos obter o valor de por semelhança de triângulos: (2 ) ( ) ( ) ⁄ Lembremos agora das relações verificadas anteriormente:
- 3. Diego Arley 25 ( ) { (2) 2 (3) 3 A partir de (2), temos que: Logo, substituindo o em (3): 2 2 3 Assim, temos a seguinte matriz organizada em colunas, respectivamente, por: tempe- ratura absoluta, pressão, volume. Cada linha representa um dos pontos (A, B e C). 25 2 [2 ] 3 Com isso, podemos calcular a variação de energia interna (∆ ) total, somando as variações parciais: ∆ ∆ ∆ ∆ 2 ∆ 2 ∆ ∆ 2 ( ) ∆ 2 ( ) ∆ 2 (3 25) ∆ 2 2 5 ∆ ∆ Agora, calculamos o trabalho realizado pelo gás nas transformações mostradas pelo diagrama: ( 2 )(3 ) ( )( ) 2 5 3
- 4. Diego Arley Finalmente, através a 1ª Lei da Termodinâmica, podemos obter o calor trocado no processo : ∆ 3 3 Porém, é necessário converter as unidades, visto que o enunciado do exercício pede que a resposta final seja dada em quilocaloria, e não em Joule ou múltiplo deste. Diego Arley
