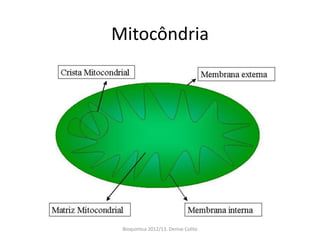
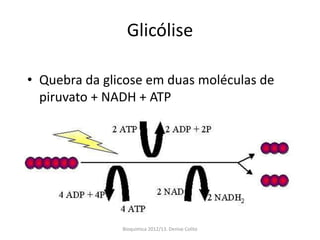
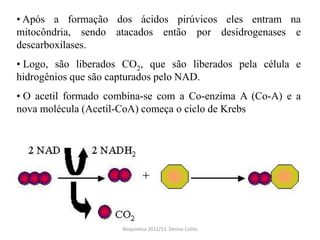
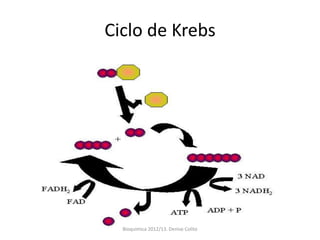
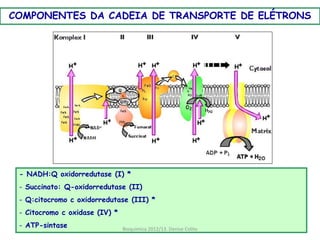
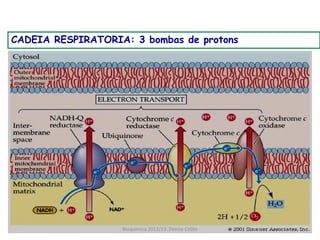
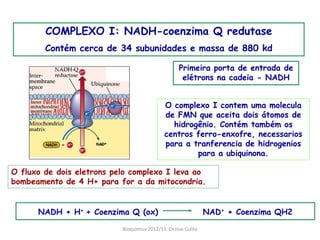
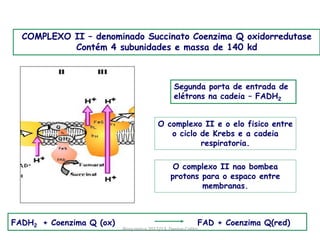
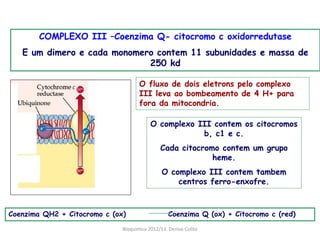
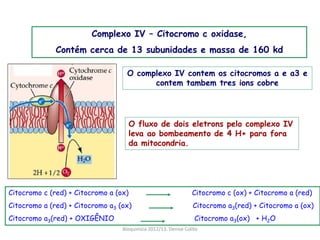
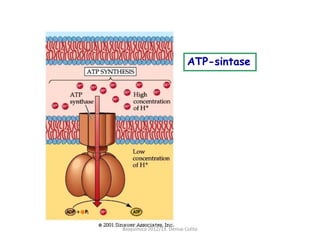
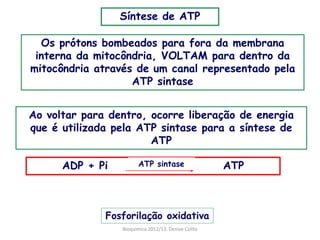
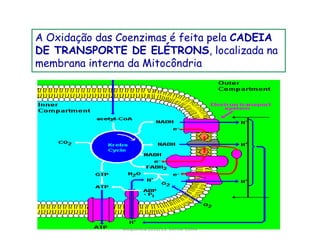
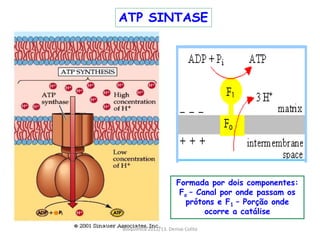
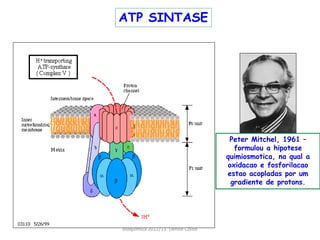
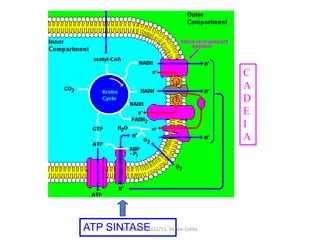
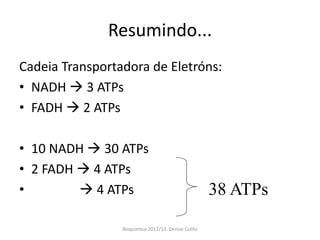
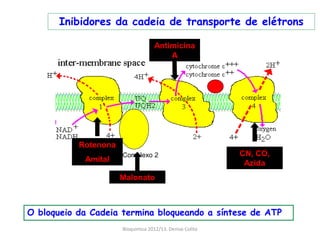
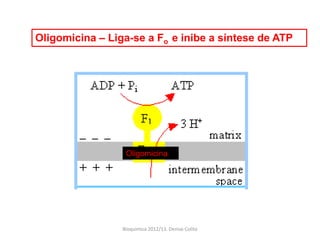
A respiração celular ocorre em duas fases principais: a anaeróbia (glicólise) que ocorre no citoplasma e a aeróbia (ciclo de Krebs e cadeia transportadora de elétrons) que ocorre dentro da mitocôndria. A cadeia transportadora de elétrons bombeia prótons através da membrana mitocondrial interna, criando um gradiente eótico que é usado pela ATP sintase para sintetizar ATP a partir de ADP e fosfato inorgânico.