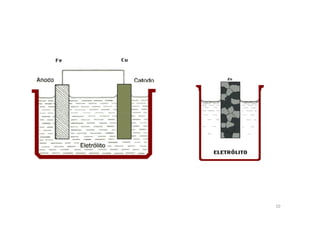
O documento discute os principais tipos de corrosão e seus mecanismos. Apresenta os casos mais comuns de corrosão, como a atmosférica e galvânica, e descreve os mecanismos de corrosão químico, físico e eletroquímico. Explica que a corrosão eletroquímica envolve a formação de uma célula eletroquímica espontânea através de processos anódico e catódico.