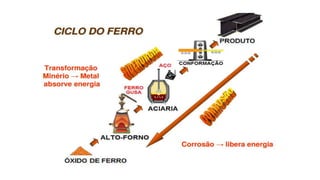
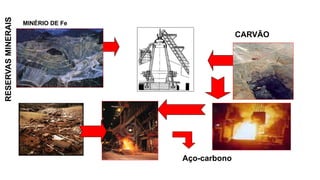
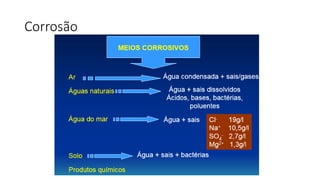
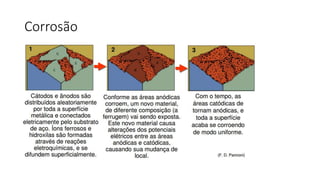
1. O documento discute os conceitos e tipos de corrosão metálica, incluindo corrosão química e eletroquímica.
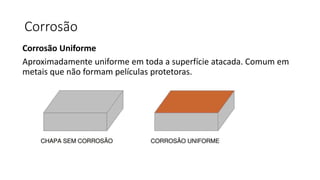
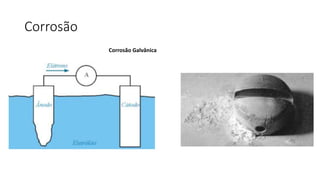
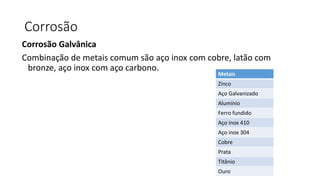
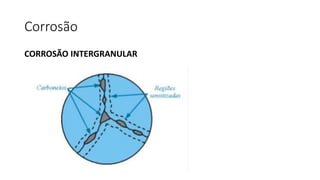
2. São descritos os tipos fundamentais de corrosão como uniforme, galvânica, em frestas e por pites.
3. A corrosão causa grandes perdas econômicas e problemas ambientais, e diferentes métodos podem ser usados para combatê-la, como proteção catódica, revestimentos e uso de inibidores.