Lista 3
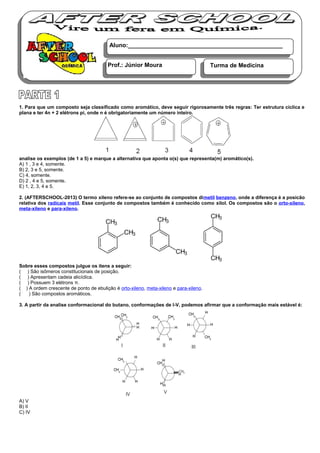
- 1. 1. Para que um composto seja classificado como aromático, deve seguir rigorosamente três regras: Ter estrutura cíclica e plana e ter 4n + 2 elétrons pi, onde n é obrigatoriamente um número inteiro. analise os exemplos (de 1 a 5) e marque a alternativa que aponta o(s) que representa(m) aromático(s). A) 1 , 3 e 4, somente. B) 2, 3 e 5, somente. C) 4, somente. D) 2 , 4 e 5, somente. E) 1, 2, 3, 4 e 5. 2. (AFTERSCHOOL-2013) O termo xileno refere-se ao conjunto de compostos dimetil benzeno, onde a diferença é a posicão relativa dos radicais metil. Esse conjunto de compostos também é conhecido como xilol. Os compostos são o orto-xileno, meta-xileno e para-xileno. Sobre esses compostos julgue os itens a seguir: ( ) São isômeros constitucionais de posição. ( ) Apresentam cadeia alicíclica. ( ) Possuem 3 elétrons π. ( ) A ordem crescente de ponto de ebulição é orto-xileno, meta-xileno e para-xileno. ( ) São compostos aromáticos. 3. A partir da analise conformacional do butano, conformações de I-V, podemos afirmar que a conformação mais estável é: A) V B) II C) IV Aluno:_______________________________________________ Prof.: Júnior Moura Turma de Medicina
- 2. D) III E) I 4. (AFTERSCHOOL-2013) As projeções de Newman são uma alternativa conveniente para ilustrar os conformêros do etano. Podemos transformar uma molécula desenhada com a notação em linhas tracejadas e cunhas em uma projeção de Newman. Observe as conformações abaixo: Assinale a ordem decrescente de energia: A) I > II > III > IV B) I > III > II > IV C) III > II > I > IV D) IV > III > II > I E) IV > I > II > III 1. (AFTERSCHOOL – 2013) Faça o balanceamento da seguinte equação, cuja reação química ocorre em meio ácido e assinale a reação global balanceada: Cr2O7 + Fe2+ Cr3+ + Fe3+ A) 8Fe+2 + 14H+ +Cr2O7 8Fe+3 + 2Cr+3 + 7H2O B) Fe+2 Fe+3 C) 8e- + 14H+ + Cr2O7 2Cr+3 + 7H2O D) Cr2O7 + 3Fe2+ 2Cr3+ + Fe3+ E) 8Fe+2 + 7H+ +Cr2O7 4Fe+3 + 2Cr+3 + 7H2O 2. (AFTERSCHOOL - 2013) Faça o balanceamento da seguinte equação, cuja reação química ocorre em meio ácido e assinale a reação global balanceada: Fe+2 + SO4 -2 Fe+3 + SO3 -2 A) 3Fe+2 + SO4 -2 2Fe+3 + SO3 -2 B) 3Fe+ 2Fe+3 C) 2Fe+2 + SO4 -2 + 2H+ 2Fe+3 + SO3 -2 + H2O D) SO4 -2 SO3 -2 E) Fe+2 + SO4 -2 + 6H+ Fe+3 + SO3 -2 + 6H2O 3. (FACID) A uma amostra de 1,00 g de um minério de ferro acrescenta-se uma quantidade conveniente de uma solução aquosa de ácido clorídrico. A solução resultante é de ferro na forma de Fe2+ (aq). Para oxidar todo o Fe2+ para Fe3+ foi exigido 30,00 mL de uma solução 0,05 mol/L de persulfato de potássio, K2S2O8. A equação iônica, em meio ácido, está representada abaixo: Fe 2+ (aq) + S2O8 2- (aq) SO3 2- (aq) + Fe 3+ (aq) Assinale a alternativa que apresenta o percentual de ferro no minério. A) 12,90% B) 21,06% C) 32,50% D) 50,40% E) 66,50%
