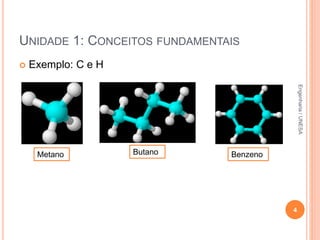
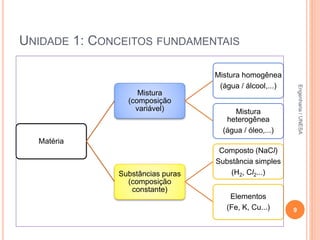
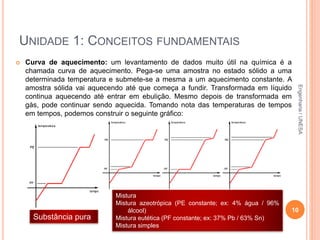
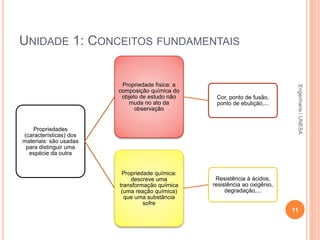
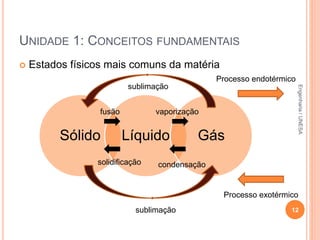
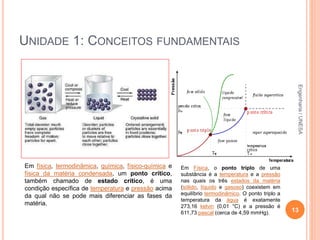
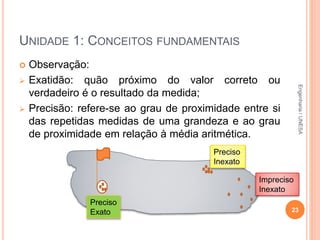
O documento resume os principais conceitos fundamentais da química, incluindo: 1) a definição de química como o estudo da composição e propriedades da matéria; 2) as estruturas básicas da matéria como átomos e moléculas; 3) os diferentes estados físicos da matéria e as transformações entre eles; 4) a distinção entre propriedades intensivas e extensivas.