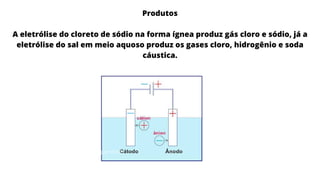
O documento descreve o que é eletrólise, o processo de decomposição de compostos químicos através de uma corrente elétrica induzida. Explica que a eletrólise é uma reação de oxirredução não-espontânea que produz diferentes gases dependendo do composto químico, e descreve dois tipos principais de eletrólise: eletrólise ígnea de substâncias iônicas fundidas e eletrólise aquosa de soluções aquosas.