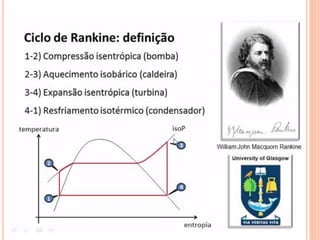
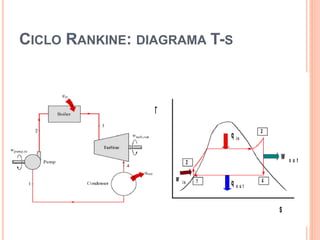
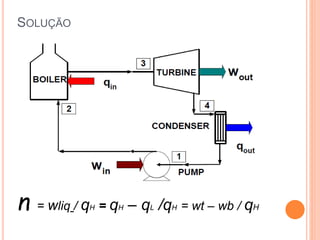
O documento discute ciclos termodinâmicos como o Ciclo de Carnot e o Ciclo de Rankine. O Ciclo de Rankine converte calor em trabalho usando vapor de água e é usado em 90% da geração de energia elétrica no mundo. O documento fornece um exemplo de como calcular o rendimento de um ciclo de Rankine.