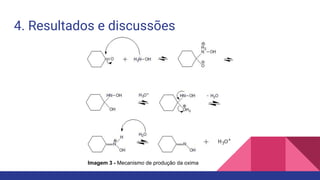
O documento descreve a síntese e purificação da ciclohexanona-oxima através da reação da ciclohexanona com o cloridrato de hidroxilamina na presença de carbonato de sódio. O produto obtido foi impuro, contendo ciclohexanona residual, como mostrado pela cromatografia em camada delgada e ponto de fusão. Processos adicionais de purificação são necessários para remover as impurezas.






![4. Resultados e discussões
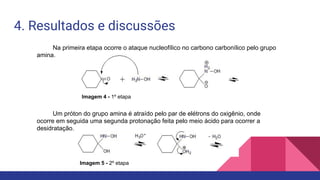
A hidroxilamina quando em solução entra em equilíbrio com o seu ácido conjugado
[H3
OH]+
que por sua vez não reage com a ciclohexanona, portanto utilizamos o cloridrato
de hidroxilamina (H3
OHCl) que reagirá aos poucos com Carbonato de sódio (Na2
CO3
)
para liberar a hidroxilamina. Como podemos ver abaixo:
2NH2
OH . HCl + Na2
CO3
NH2
OH + 2NaCl + H2
CO3
O ácido carbônico formado será usado como catalisador ácido para a reação com a
ciclohexanona.
Imagem 2 - Reação do cloridrato de hidroxilamina com o carbonato de sódio](https://image.slidesharecdn.com/relatorio-180426172441/85/Relatorio-Ciclo-Hexanona-8-320.jpg)