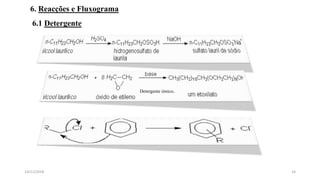
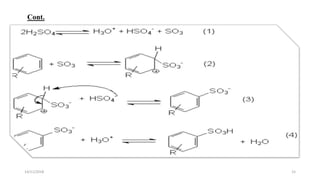
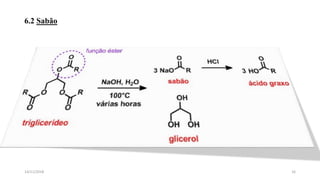
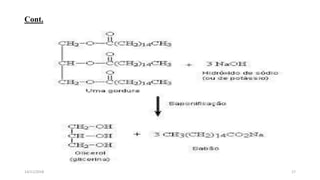
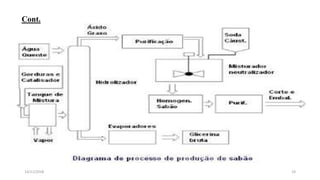
O documento aborda a produção de sabão e detergente, descrevendo suas composições químicas, processos de fabricação e diferenças entre os dois produtos. Explora também a metodologia e as matérias-primas utilizadas tanto na produção caseira quanto industrial, bem como as vantagens e desvantagens de cada tipo. Adicionalmente, discute os efeitos dos tensoativos, sua toxicidade e a importância na redução da tensão superficial dos líquidos.