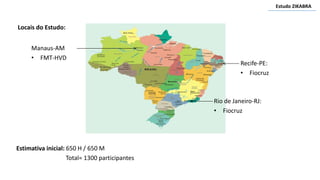
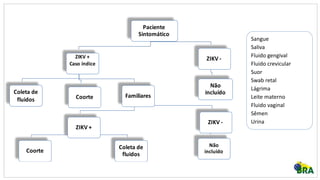
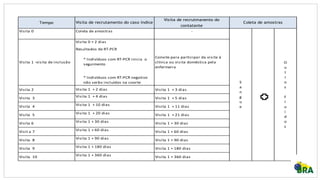
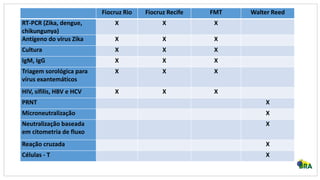
Este estudo avaliará a persistência do vírus Zika em fluidos corporais de pacientes infectados no Brasil por até 12 meses. Amostras de sangue, sêmen e outros fluidos serão coletadas periodicamente de 1.300 participantes em três cidades e testadas para detecção de RNA, anticorpos e isolamento viral. Os resultados fornecerão evidências sobre o período em que o vírus permanece ativo em diferentes fluidos e fatores que influenciam sua persistência, para orientar recomendações sobre prevenção de transmissão.