[1] O documento descreve os conceitos fundamentais de pHmetria, incluindo o que é pH, teorias de ácidos e bases, íon hidrogênio, escala de pH e pOH, sistemas tampão e métodos de medição de pH.
[2] Os principais tópicos abordados são a definição de pH, teorias de ácidos e bases, escala logarítmica de pH e pOH, funcionamento de sistemas tampão, e métodos colorimétrico e potenciométrico para medição de pH.
[3

![Íon Hidrogênio
→ É um núcleo positivo de um átomo de hidrogênio que perdeu
seu único elétron.
H+
⮃
H3O+
→ Por ser uma partícula pequena e com uma carga positiva, o íon
H+ é altamente reativo.
→ Em solução aquosa ele se hidrata, ou seja se combina com o
oxigênio (parcialmente negativo) da molécula de água.
+ H2O
Íon hidrônio ou hidroxônio
Para fins didáticos: [ H3O+] = [H+]](https://image.slidesharecdn.com/aulaphmetria2020-240218194905-303de710/85/Aula-pHmetria-apresentacao-da-aula-pratica-4-320.jpg)

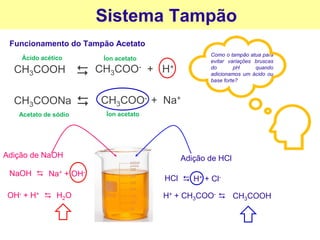
![Acidez e basicidade
→ A acidez e a basicidade (alcalinidade) de uma solução aquosa
dependem das concentrações de H+ e OH- presentes na solução.
[H+] > [OH−] Caráter Ácido
[H+] = [OH−] Caráter Neutro
[H+] < [OH−] Caráter Básico ou alcalino
Como surgiu o pH?](https://image.slidesharecdn.com/aulaphmetria2020-240218194905-303de710/85/Aula-pHmetria-apresentacao-da-aula-pratica-6-320.jpg)
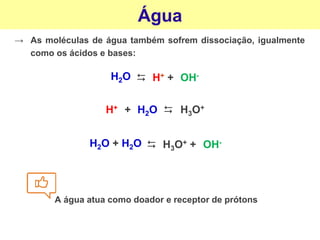
![A ionização da água e sua relação com o pH
→ A água pura apresenta quantidades pequenas, porém iguais, de íons
H+ (ou H3O+) e OH- sendo, portanto, uma solução neutra.
OH-
⮃
H2O H+ +
Aplicando a Lei da ação das massas:
Produto iônico da água
[H+] = 10-7 M
[OH-] = 10-7 M
1,8 x 10-16 M 55,55 M](https://image.slidesharecdn.com/aulaphmetria2020-240218194905-303de710/85/Aula-pHmetria-apresentacao-da-aula-pratica-8-320.jpg)
![pH e pOH
→ Devido as baixas concentração de H+ e OH- nas soluções aquosas, em
1909 o pesquisador dinamarquês Søren Sørensen desenvolveu a
escala de pH (potencial hidrogeniônico) e de pOH (potencial
hidroxiliônico), medida de acidez e basicidade das soluções.
pH = - log [H+] pOH = - log [OH-]
pH + pOH = 14](https://image.slidesharecdn.com/aulaphmetria2020-240218194905-303de710/85/Aula-pHmetria-apresentacao-da-aula-pratica-9-320.jpg)

![pH e pOH
Exemplos:
1) Calcule o pH de uma solução que tem concentração de íons H+ igual a 10-4 M:
pH = - log [H+] pH = - log 10-4
pH = - (-4)log 10
= 1
pH = 4
2) Calcule o pOH de uma solução que tem concentração de íons OH- igual a 10-12 M:
pOH = - log [OH-] pOH = - log 10-12 pOH = 12
3) Calcule o pH de uma solução que tem concentração de íons OH- igual a 10-8 M:
pOH = - log [OH-] pOH = - log 10-8 pOH = 8
pH + pOH = 14 pH + 8 = 14 pH = 14 - 8 pH = 6](https://image.slidesharecdn.com/aulaphmetria2020-240218194905-303de710/85/Aula-pHmetria-apresentacao-da-aula-pratica-11-320.jpg)
![pH e pOH
Exemplos:
4) Calcule o pH e o pOH de uma solução que [H+] igual a 8,1 x 10-7 M:
pH = - log [H+] pH = - log 8,1 x 10-7
Aplicar propriedade do
logaritmo do produto
log (a ∙ b) = log a + log b
pH = - (log 8,1 + log 10-7) pH = - log 8,1 - log 10-7
Sabendo que log 8,1 = 0,91, então fica:
pH = - 0,91- (-7) pH = - 0,91+ 7 pH = 6,09
Para calcular o pOH, é só lembrar que pH + pOH = 14
pH + pOH = 14 6,09 + pOH = 14 pOH = 14 - 6,09
pOH = 7,91](https://image.slidesharecdn.com/aulaphmetria2020-240218194905-303de710/85/Aula-pHmetria-apresentacao-da-aula-pratica-12-320.jpg)
![pH e pOH
Para treinar:
1) Calcule o pH de uma solução que tem [H+] igual a 2,8 x 10-12 mol/L:
Dado: log 2,8 = 0,45.
2) Calcule o pH de uma solução que tem [OH-] igual a 1,75 x 10-5 mol/L:
Dado: log 1,75 = 0,24.
Resposta: pH = 11,55
Resposta: pH = 9,24](https://image.slidesharecdn.com/aulaphmetria2020-240218194905-303de710/85/Aula-pHmetria-apresentacao-da-aula-pratica-13-320.jpg)







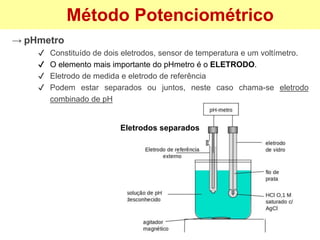

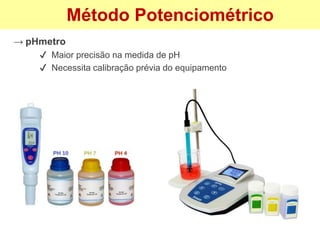
![→ pHmetro
✔ Medida: através do eletrodo combinado,
mede a diferença de potencial elétrico
(d.d.p.) entre duas soluções separadas por
uma membrana de vidro especial, com
diferentes concentração de H+, e converte o
resultado em pH
✔ Equação de Nernst
Método Potenciométrico
H+
H+
H+
H+
H+
H+
OH-
OH-
OH-
OH-
ddp = diferença de potencial elétrico através da membrana de vidro seletiva
z = valência do íon
F = constante de Faraday (96500 Coulomb/mol)
R = constante dos gases perfeitos (8,3143 J/(K⋅mol)
T = temperatura absoluta (K)
[Hi] = concentração de H+ no interior
[He] = concentração de H+ na solução](https://image.slidesharecdn.com/aulaphmetria2020-240218194905-303de710/85/Aula-pHmetria-apresentacao-da-aula-pratica-26-320.jpg)