Química Orgânica: Evolução da Teoria e Conceitos Fundamentais
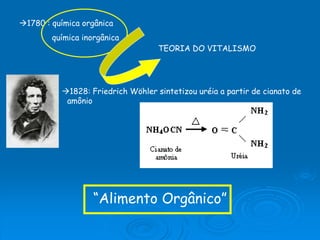
- 1. 1780 : química orgânica química inorgânica TEORIA DO VITALISMO 1828: Friedrich Wöhler sintetizou uréia a partir de cianato de amônio “Alimento Orgânico”
- 2. Regra do Octeto Um átomo estará estável quando sua camada de valência possuir 8e-, assemelhando-se à configuração eletrônica de um gás nobre (exceção H e He - 2e-) - Ligações iônicas - Ligações covalentes - Ligações dativas
- 3. Carbono É a base da química orgânica: os compostos orgânicos são formados basicamente de carbono ligado a outros elementos: H, N, O,S, Cl, etc Nos compostos orgânicos os átomos podem formar um número fixo de ligações; a medida dessa habilidade é chamada valência. O CARBONO é tetravalente.
- 4. Tipos de ligações do carbono Saturado x insaturado; Cadeia aberta x cadeia fechada Normal x ramificada; Homogênea x heterogênea; Alicíclica x aromática
- 5. Geometria molecular O arranjo tri-dimensional dos átomos em uma molécula geometria molecular A teoria da repulsão dos pares de elétrons (ligantes e não-ligantes) procura explicar o arranjo dos átomos numa molécula.
- 6. Teoria da repulsão dos elétrons Electrons são cargas carregadas negativamente, portanto se repelem mutuamente. Os elétrons ocuparão posições tais que minimizem os efeitos de suas repulsões (ocupando regiões o mais afastado possível uns dos outros). Num átomo os elétrons ocupam determinados espaços chamados orbitais (máximo 2e num orbital). Tipos de orbitais mais comuns: orbitais s ; p ;
- 11. Funções Químicas Alcanos, alcenos, alcinos, alcadienos; Cicloalcanos, ciclenos, ciclodienos;
- 12. Funções Químicas Alcool,fenol, cetona; Aldeído, ac. carboxílico, éster
- 13. Funções Químicas Aminas e amidas; Éter
- 14. Isomeria Isomerismo ou Isomeria (iso = mesmo , meros = partes) é o fenômeno caracterizado pela existência de duas ou mais substâncias diferentes que apresentam fórmulas químicas idênticas, porém diferentes fórmulas estruturais. Isomeria constitucional Isomeria espacial
- 15. Isomeria constitucional - De função - De posição - De cadeia
- 16. Isomeria constitucional - Tautomeria - De compensação ou metameria
- 17. Isomeria espacial - geométrica - óptica Cis = do mesmo lado Trans = de lados opostos Destrógiros (D) = desviam a luz plano- polarizada para a direita Levógiros (L) = desviam para a esquerda Mistura Quiral =
