005 enzimas 2011_2_002
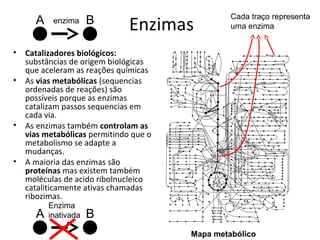
- 1. Enzimas Cada traço representa A enzima B uma enzima • Catalizadores biológicos: substâncias de origem biológicas que aceleram as reações químicas • As vias metabólicas (sequencias ordenadas de reações) são possíveis porque as enzimas catalizam passos sequencias em cada via. • As enzimas também controlam as vias metabólicas permitindo que o metabolismo se adapte a mudanças. • A maioria das enzimas são proteínas mas existem também moléculas de acido ribolnucleico cataliticamente ativas chamadas ribozimas. Enzima A inativada B Mapa metabólico
- 2. Atividade enzimática • A atividade enzimática é quanto produto é enzima produzido na presença da enzima por A B A B unidade de tempo em condições químicas A B A A definidas (temperatura, pH, composição de A B B B sais...): A B A B A A B B mmol / segundo . Enzima 2 (milimol de produto por segundo) A B Ou mais freqüentemente: A B µmol /minuto A B A A B (micromol de produto por minuto) A B B A B A B A A B B
- 3. Regulação da atividade enzimática 1. Regulação pelo produto (feedback negativo) 1.1 – Inibição pelo produto imediato da enzima Sítio regulador 1.2 – Inibição pelo produto final da via S Enzima P Quando produto da Quando o produto se liga ao via se liga à enzima sítio regulador inativa a enzima regulatória da via inibe sua atividade... Enz. S Enzima 1 A Enz. 2 B Enz 3 C 4 P ...e, por conseqüência, inibe a via Via metabólica
- 4. Regulação da atividade enzimática 2 - Regulação por fosforilação-defosforilação ciclo fosforilação-defosforilação forma ATP cinase ADP Forma defosforilada fosforilada fosforilação OH OPO3-2 Enzima Enzima Forma ativa defosforilação Forma inativa (ou forma inativa) (ou forma ativa) fosfatase PO4-3 Cinase: enzima regulatória que fosforila outras enzimas Fosfatase: enzima regulatória que defosforila outras enzimas A fosforilação é uma modificação covalente reversível
- 5. Classes de enzimas • Existem mais de 2000 enzimas conhecidas até hoje • Um sistema de classificação foi desenvolvido com base no tipo de reação • Todas enzimas estão catalogadas num cadastro formado por quatro números separados por pontos(EC- de “enzime comission”. Ex.:1.13.11.11 ). • O primeiro indica a qual das seis grandes classes de proteínas ela pertençe • Os dois seguintes indicam sub-classe e sub-subclasse • O último indica qual é a enzima propriamente dita
- 6. As seis grandes classes de enzimas Classe Tipo de reação Sub-classes
- 7. Ex: lactatato desidrogenase: EC no: 1.1.1.27 Piruvato Lactato NAD reduzido NAD oxidado • Classe 1 (Oxiredutase) • Subclasse 1.1: Grupamento CH-OH como doador de elétron • Sub-subclasse 1.1.1: NAD(P)+ como aceptor de elétron • Enzima número 1.1.1.27: lactato desidrogenase
- 8. Catálise Enzimática • Enzimas são catalizadores muito eficientes • Podem aumentar a velocidade de uma reação em até 1017 vezes(1017= 100.000.000.000.000.000) Exemplos de algumas enzimas e o aumento na velocidade de reação causado por cada uma delas
- 9. Reação não catalizada água de hidratação • Para comprender os mecanismos envolvidos na catálise enzimática vamos antes observar uma reação não catlizada: A+B C+D • Em solução, os reagentes A e B encontram-se hidratados e movem-se randomicamente. • Para que reagam é nescessário que colidam de forma favorável (colisão efetiva) • Quando colidem o complexo A-B passa por um estado de transição que requer energia para ser alcançado • Grande parte da energia de ativação é utilizada para remover parte das moléculas de água que formam a camada de hidratação em torno dos reagentes. • Em virtude desses limitantes a reação aconteçe em extensão muito pequena mesmo quando termodinâmicamente favorável.
- 10. Reação catalizada por Enzima • Enzimas são capazes de reunir os reagentes (substratos) dentro de seu centro ativo. • No centro ativo os substratos ficam numa orientação ótima para ao formação do intemediário de transição. • A ligação dos substratos ao centro ativo remove boa parte de suas camadas de hidratação. • A interação com os aminoácidos que formam o sítio ativo favorece a formação do intermendiário de transição. • Reunidos, esses fatores favorecem a formação do intermediário de transição e a reação em si.
- 11. Como a estabilização do estado de transição favoraçe a reação: um modelo intuitivo
- 12. Princípios de catálise enzimática a) Aproximação e orientação dos substratos b) Exclusão de água c) Estabilização do estado de transição d) Transferência de grupo
- 13. Cinética Enzimática • Velocidade de reação em função das concentrações dos subastratos • Determinação do Km e da Vmax • Detrminação do ótimo de pH e de temperatura • Inibidores
- 14. Cinética de Michaelis–Menten • Velocidade x concentração de substrato • Vmax: velocidade máxima • Km: concentração de substrato na qual a reação acontece na metade da velocidade máxima • Na Vmax virtualmente todas as moléculas de enzima estão com seus sitios ativos ocupados • No Km (constante de Michaelis) metade das moléculas de enzima presentes no meio de reação estão com seus sítios ocupados. • Km é uma medida da afinidade da enzima pelo substrato, quanto menor o Km maior a afinidade
- 15. Tipos de Inibidores Competitivos • Reversíveis: não causam alteração permanente na enzima, não se ligam covalentemente Não competitivos • Irreversíveis, se ligam covalentemente à enzima Alostéricos • Se ligam em um sítio diferente do sítio catalítico e alteram a afinidade da enzima Muitos inibidores são análogos do substrato natural da enzima Outros são análogos do intermediário de transição
- 16. Cinética enzimática É o estudo de como a velocidade da enzima varia em função da concentração de substrato 100µmol/min x má 100 [S] Velocidade V mmol/L µmol/min. Velocidade µmol/min. 75 0 0 0,2 25 áx /2 50 0,5 50 Vm 1,0 74 2,0 85 0,5mmol/L 25 3,0 90 4,0 94 5,0 97 0 0 6,0 99 1 2 3 4 5 6 [S] mmol/L Parâmetros cinéticos Velocidade máxima (Vmáx): é a velocidade máxima alcançada pela enzima Km: é a concentração de substrato que faz com que a enzima funcione na metade da Vmáx
- 17. Inibidores • Muitas substancias podem afetar processos metabólicos afetando a atividade de enzimas • Os inibidores de enzimas são particularmente importantes • Uma grande quntidade de remédios atuam como inibidores enzimáticos(ex: sinvastatina na síntese de colesterol, aspirina na síntese de prostaglandinas...) • Metabólitos naturais também estão envolvidos em processos regulatórios atuando como inibidores enzimáticos (mecanismo de controle por “feedback” é muito comum uma via metabólica ser inibida por seu produto final)
- 18. Vmáx não muda Sem inibidor Inibição competitiva áx 100 Velocidade µmol/min. Vm 75 Se ligam ao síto ativo mas x 2 má / Inibidor não podem ser convertidos 50 Em conc. X V em produto Inibidor Como inibidor e substrato 25 Em conc.2X competem pelo mesmo sítio esse tipo de inibição é chamado competitiva. 0 Podem ser retirados do sítio 0 1 2 3 4 5 6 ativo por um excesso de “Km aparente” [S] mmol/L substrato, portanto aumenta aumenta o Km mas não altera a velocidade máxima
- 19. Vmáx diminui Inibição não-competitiva x má V 100 O inibidor se liga de forma sem inibidor irreversível à enzima Velocidade µmol/min. x má inativando-a V 75 Atua como se diminuísse a inibidor na conc. X concentração de enzima, na x má V 50 verdade diminuí a inibidor na conc. 2X concentração de enzima ativa As moléculas que não se 25 ligaram ao inibidor funcionam normalmente, por isso o Km 0 não muda 0 Km 1 2 3 4 5 6 não muda [S] mmol/L Inibidor em Inibidor em Sem inibidor concentração X concentração 2X E E E E E-I E E-I E E-I E E E-I E EE E E E E E E-I E E E-I E E E E E E-I E E E E-I E E-I
- 20. Inibição não-competitiva • Qundo o inibidor interage com um grupamento importante para a ativiadade da enzima mas não pode ser deslocado pelo substrato a inibição é chamada não- competitiva • “Substratos suicidas” possuem um grupamento reativo que forma uma ligação covalente estável com o sítio ativo da enzima
- 21. Inibição alostérica • Inibidores alostéricos se ligam a um sítio afastado do centro ativo • Provocam uma mudança conformacional na enzima que indiretamente reduz sua atividade • Não pode ser descrito pelo modelo de Michaelis–Menten (resulta em uma sigmóide em vez de uma hipérbole)
- 22. Cinética enzimática II • As propriedades catalíticas das enzimas, consequentemente sua atividade, são influenciadas por vários fatores que devem ser otimizados e controlados para que as medidas sejam feitas de uma forma reprodutível e útil. • Esses fatores incluem: – Temperatura – pH – Força íonica (concentração de sais) – Concentrações de substratos, cofatores, inibidores
- 23. Dependência ao pH • pH ótimo • Protonação/desprotonação do sítio ativo • Em pHs extremos a proteína é inativada por desnaturação
- 24. Efeito da temperatura na atividade enzimática • O aumento de temperaura geralmente acaarreta um aumento na atividade enzimática • Até um valor de temperatura em que começa a haver desnaturação e consequente perda de atividade
