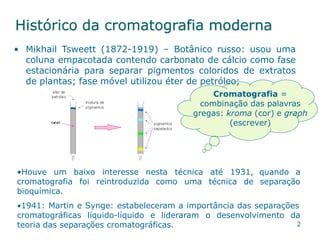
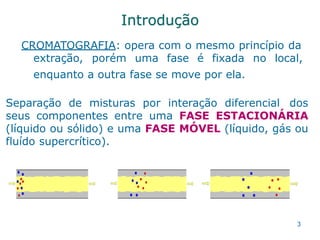
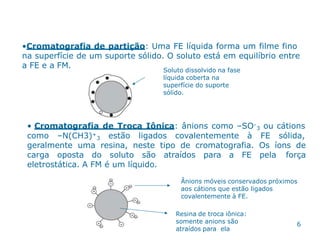
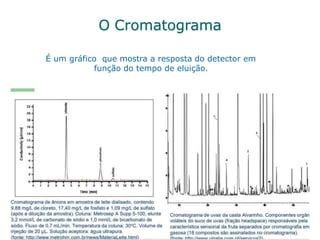
O documento descreve a história e os principais tipos de cromatografia. Resume que Mikhail Tsweett foi o primeiro a usar uma coluna empacotada para separar pigmentos de plantas em 1872. Discute que a cromatografia foi reintroduzida como técnica bioquímica em 1931 e que Martin e Synge estabeleceram a importância das separações cromatográficas líquido-líquido em 1941. Também descreve os principais tipos de cromatografia, incluindo adsorção, partição, troca iô