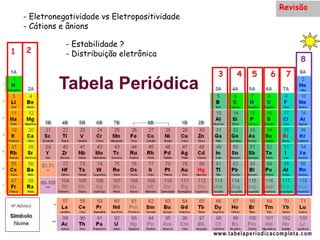
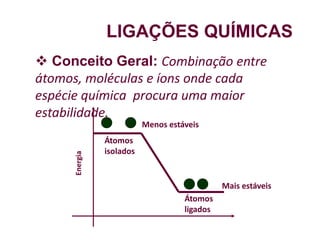
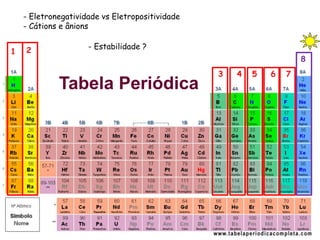
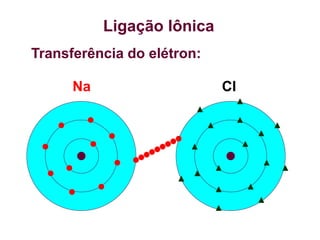
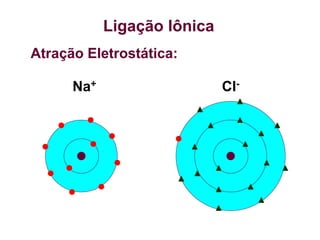
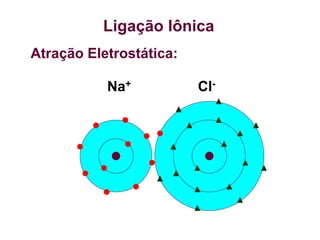
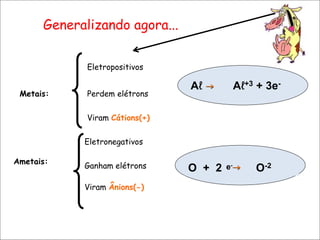
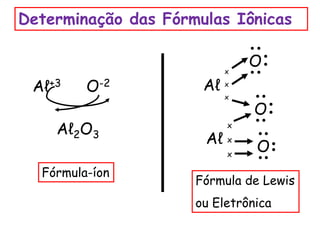
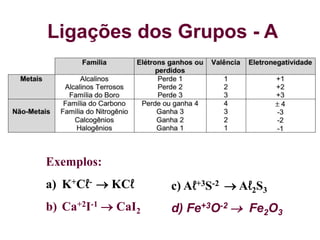
O documento aborda ligações químicas, focando na combinação entre átomos, moléculas e íons para maior estabilidade. Destaca as ligações iônicas, onde elétrons são transferidos entre átomos, originando íons de cargas opostas, e suas características como sólidos, bons condutores elétricos em solução aquosa e altos pontos de fusão. Também inclui exercícios de fixação e exemplos de ligações e fórmulas iônicas.