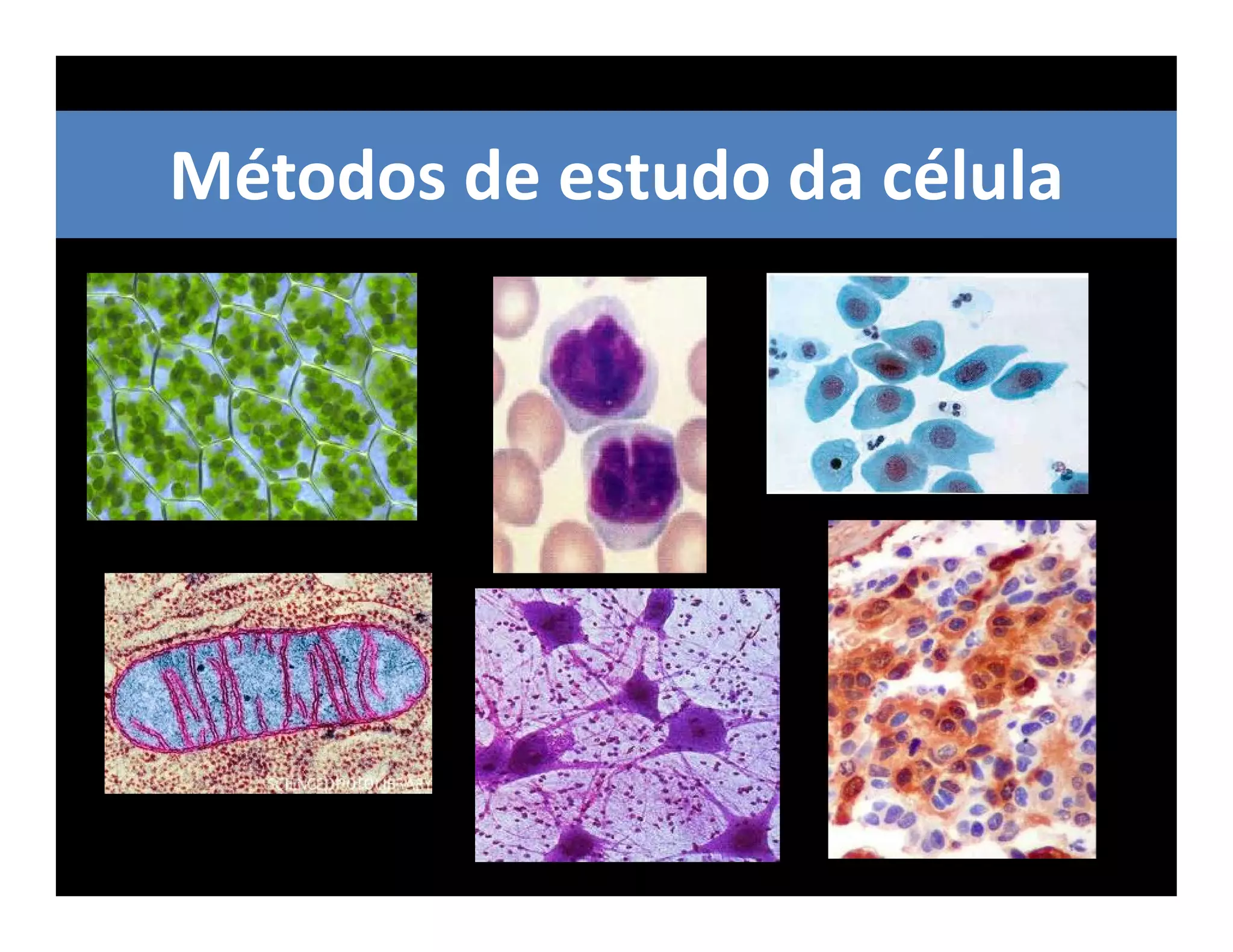
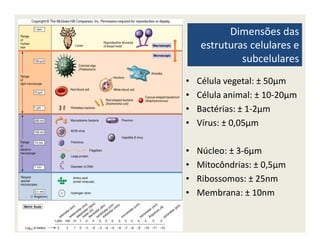
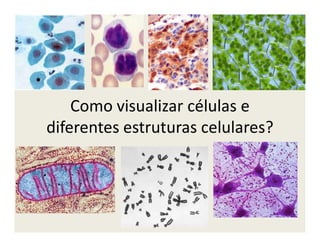
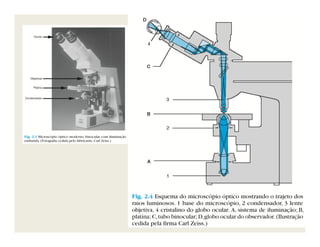
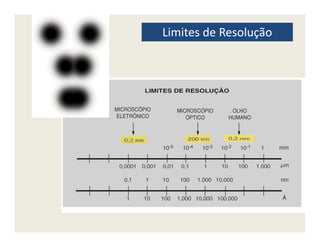
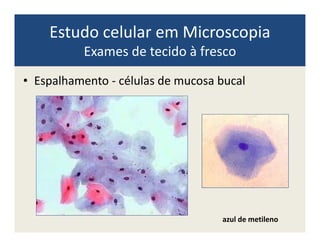
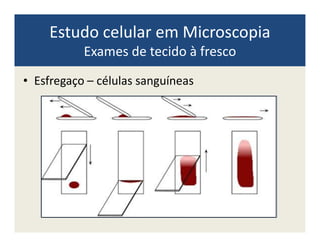
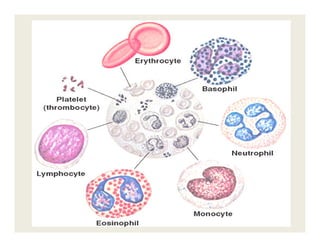
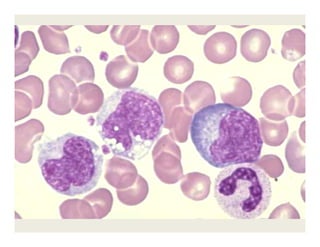
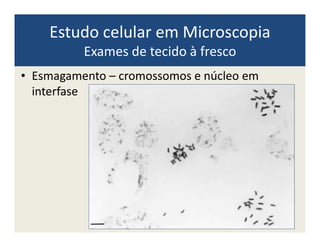
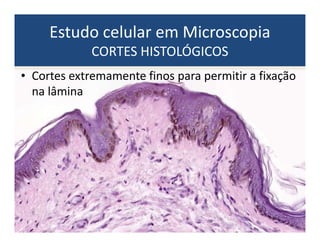
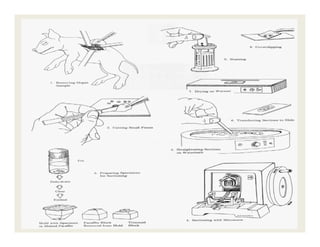
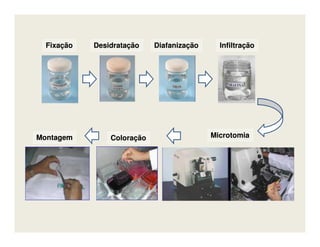
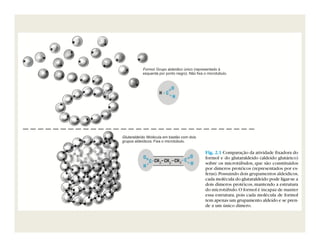
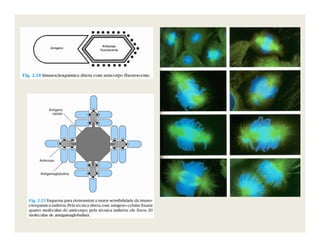
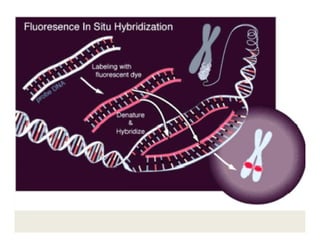
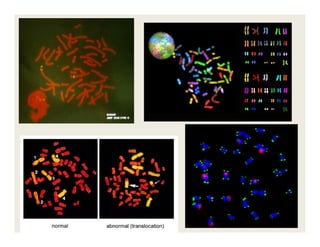
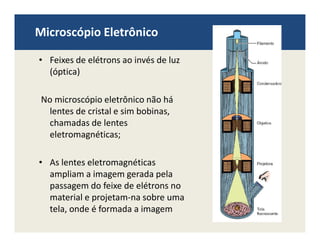
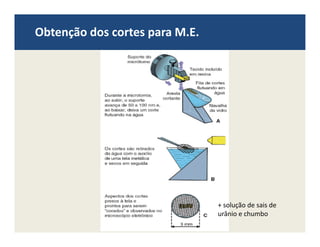
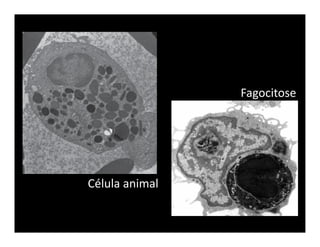
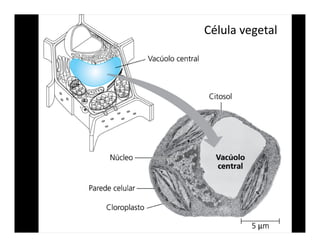
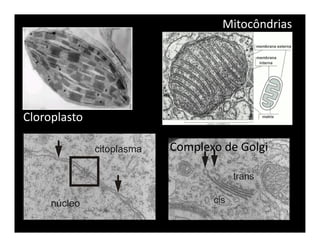
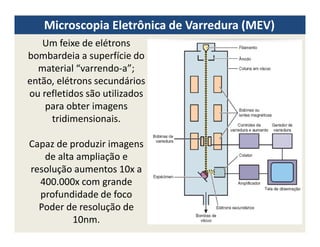
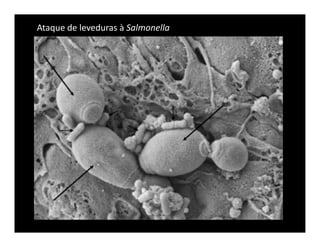
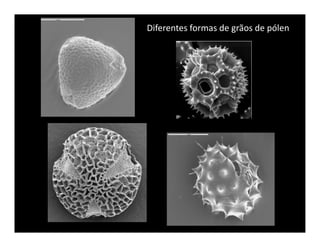
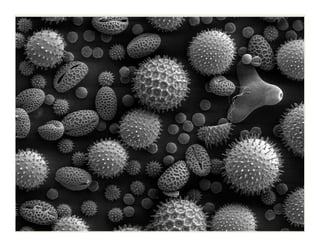
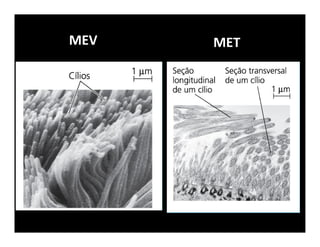
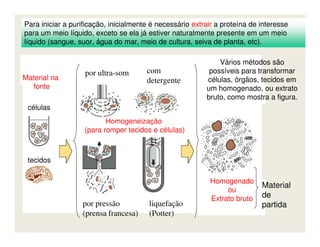
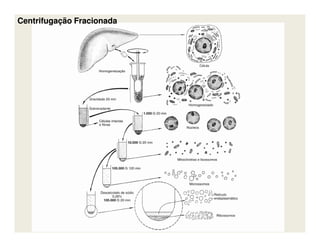
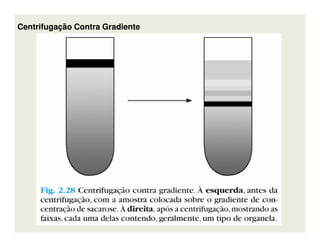
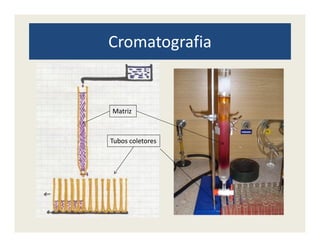
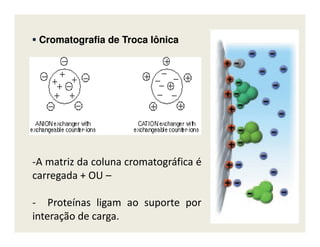
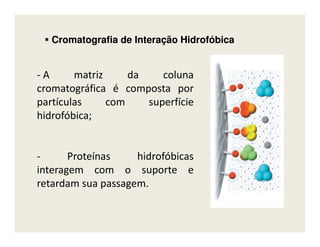
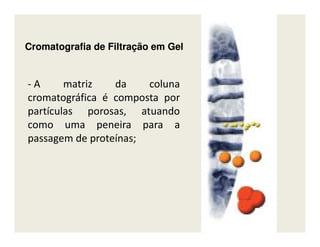
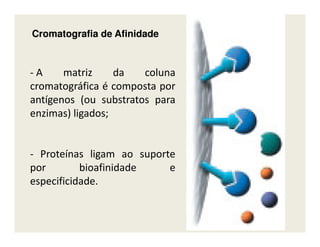
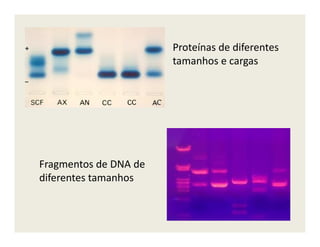
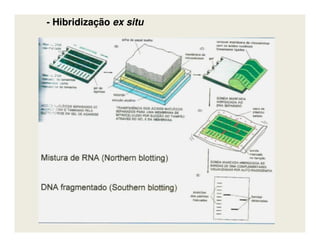
O documento descreve os principais métodos de estudo da estrutura celular, incluindo a microscopia óptica e eletrônica, técnicas de separação de organelas como centrifugação e cromatografia, e métodos de coloração para visualização de estruturas celulares.