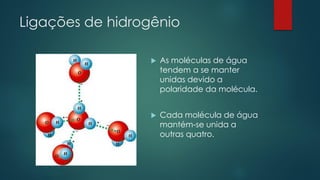
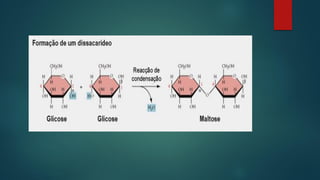
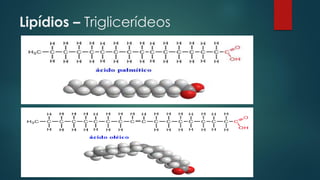
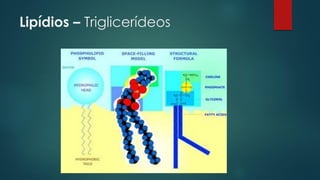
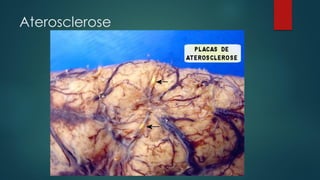
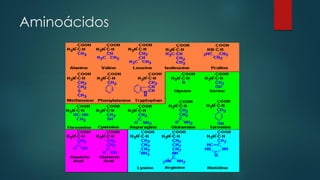
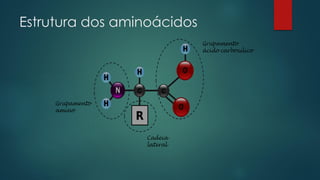
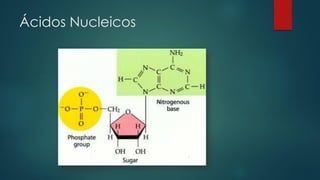
O documento discute a base química da vida, focando na água e seus papéis fundamentais nas células. A água constitui a maior parte da massa das células e possui propriedades únicas que permitem o transporte de nutrientes e o funcionamento dos processos celulares. Outros tópicos abordados incluem carboidratos, lipídios, proteínas e ácidos nucleicos, componentes essenciais das células e seus respectivos papéis.