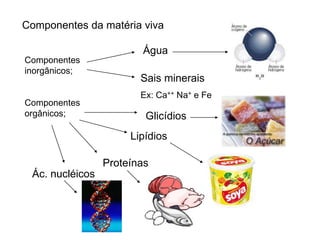
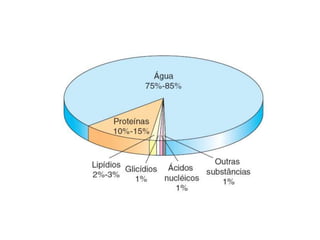
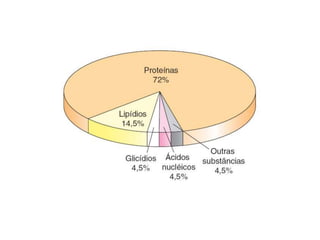
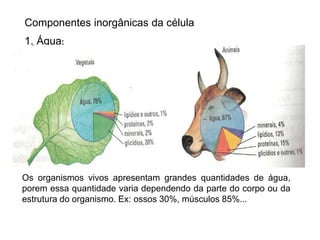
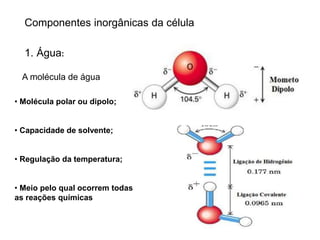
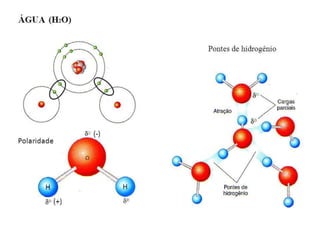
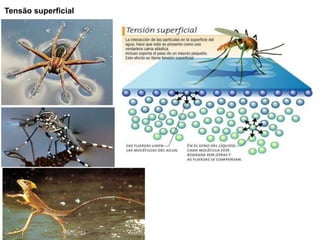
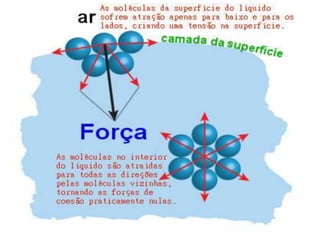
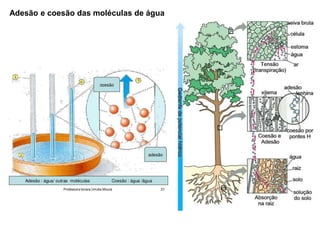
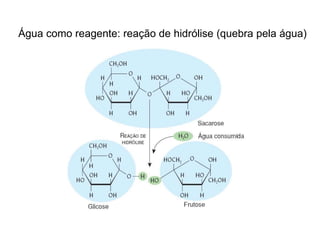
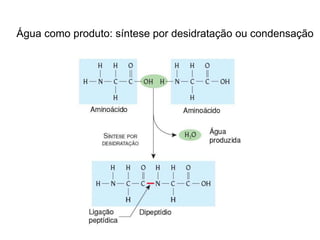
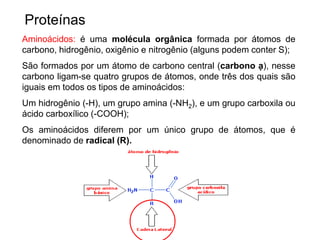
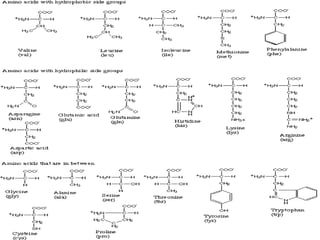
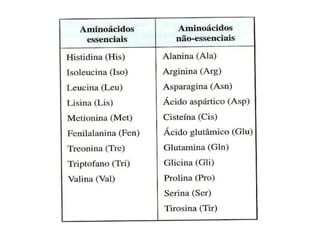
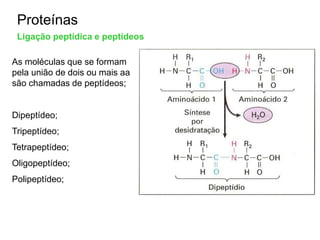
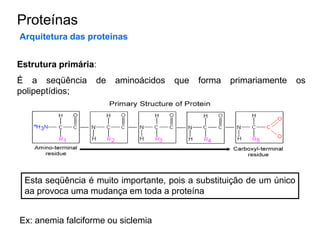
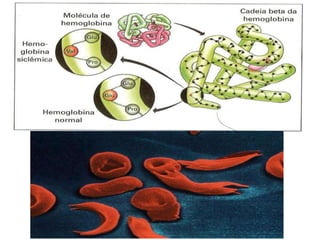
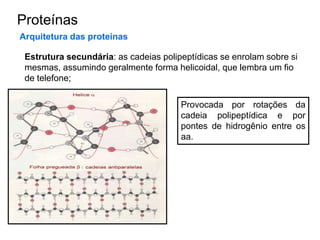
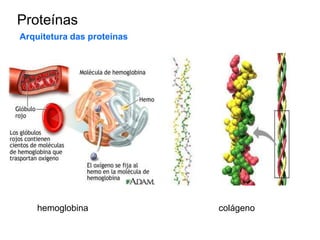
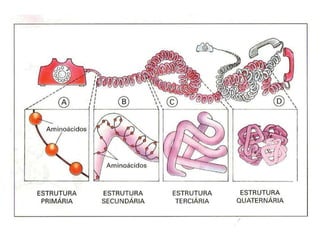
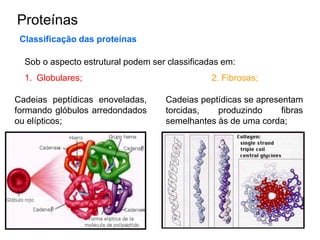
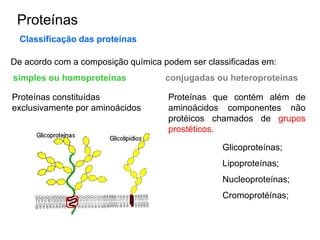
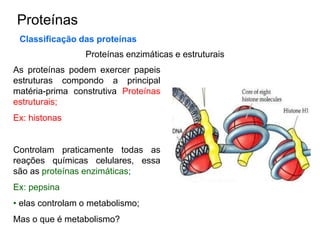
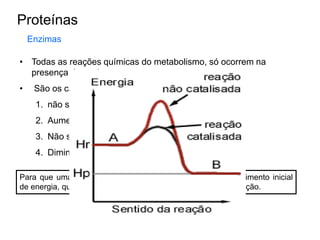
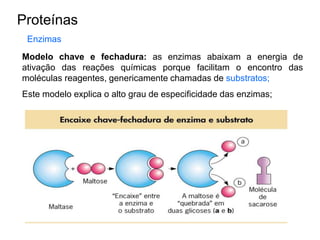
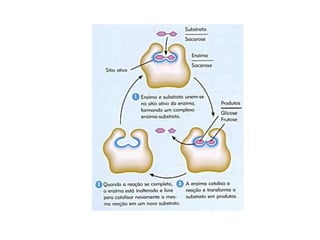
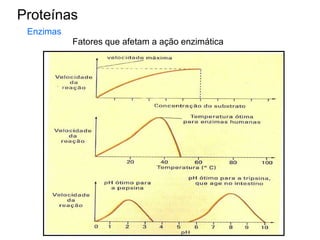
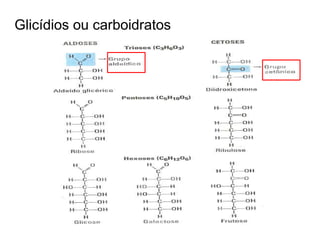
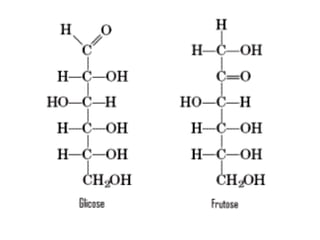
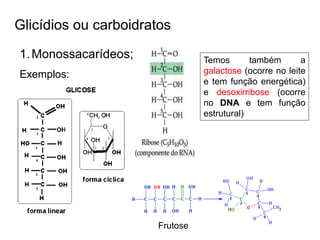
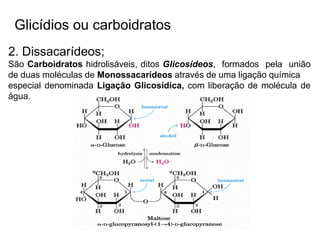
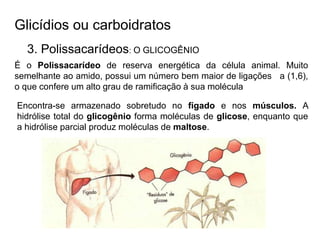
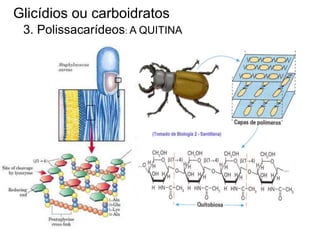
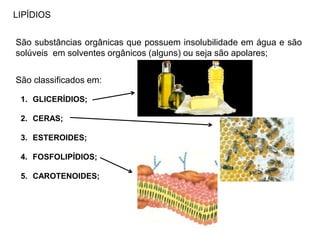
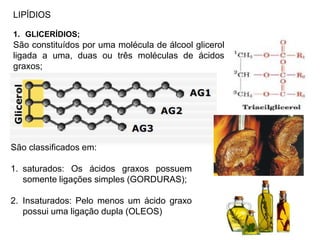
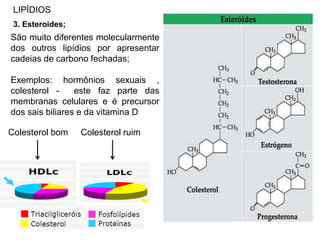
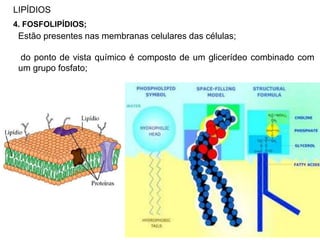
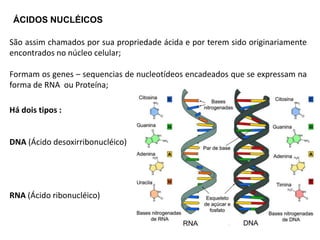
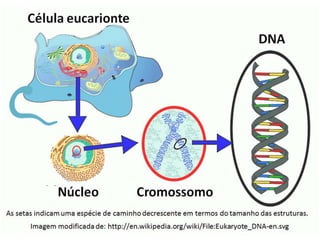
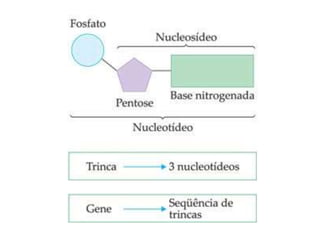
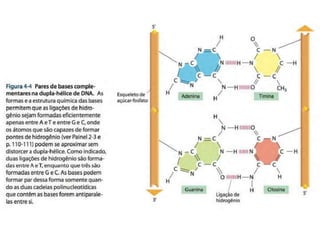
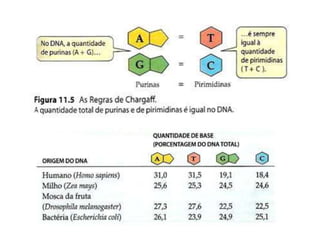
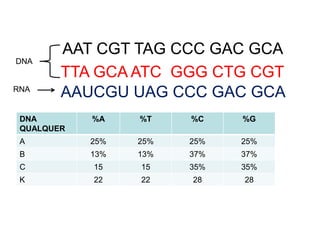
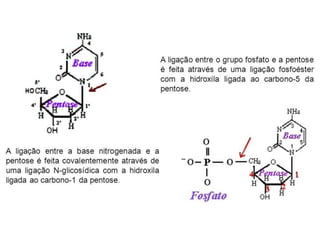
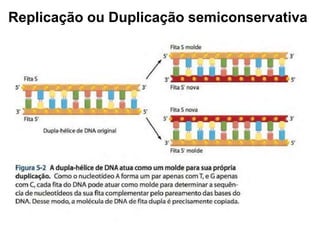
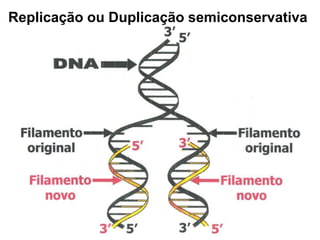
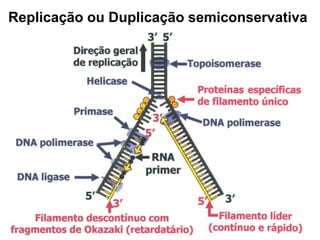
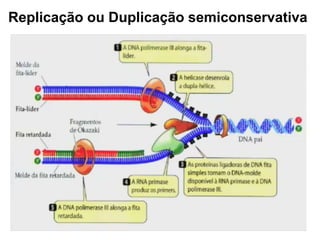
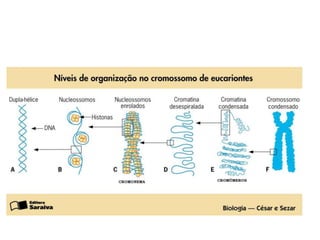
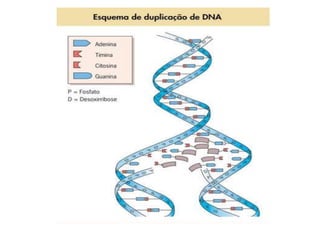
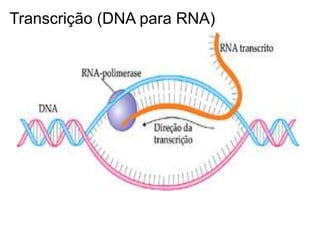
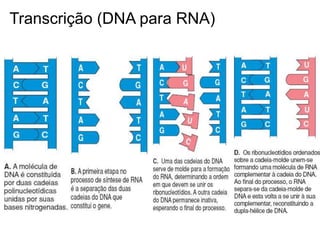
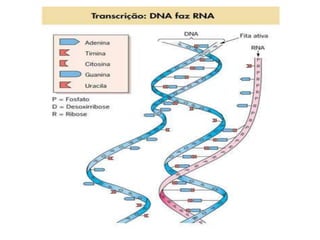
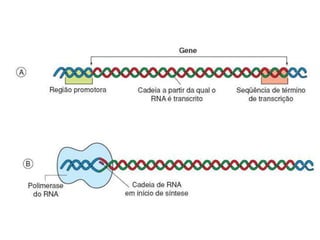
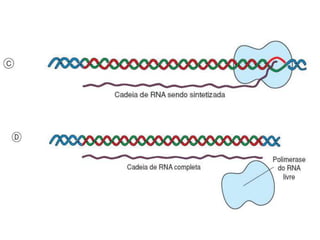
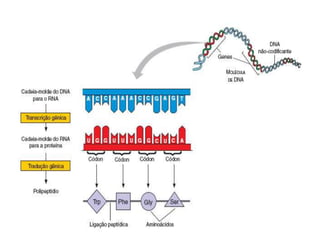
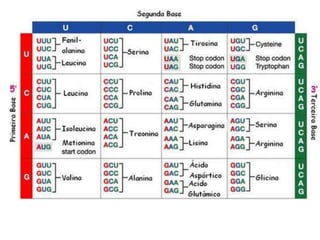
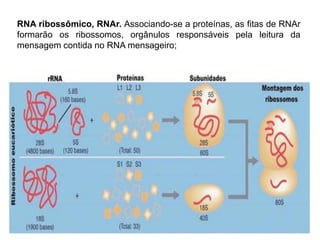
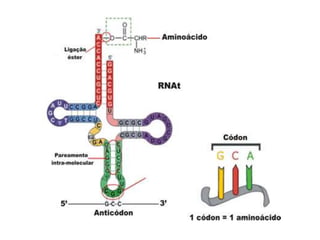
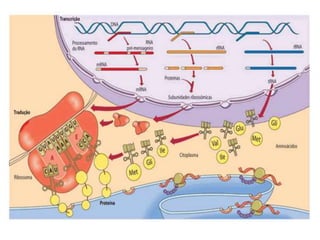
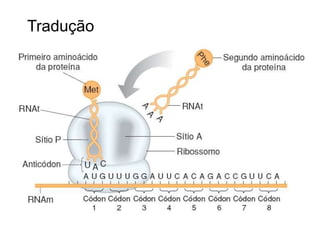
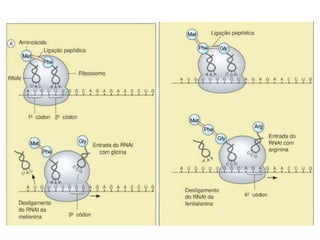
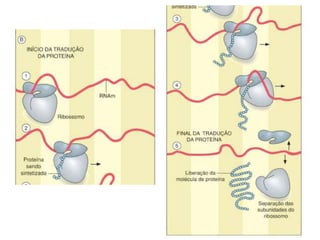
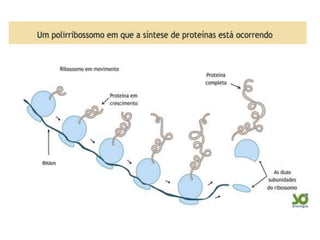
O documento aborda a composição química da célula, diferenciando componentes orgânicos, como proteínas e ácidos nucleicos, de inorgânicos, como água e sais minerais. Os principais tipos de moléculas orgânicas são analisados, incluindo a estrutura e função de proteínas e glicídios. Além disso, o texto detalha a importância do DNA e RNA na composição genética dos seres vivos.