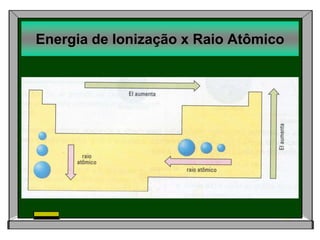
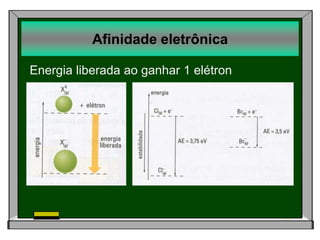
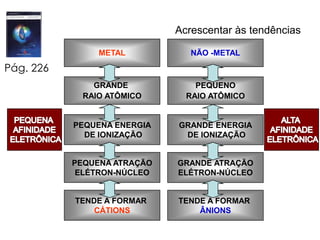
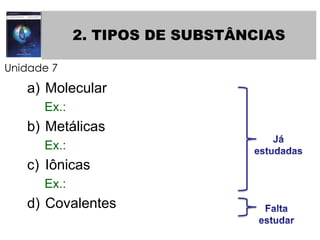
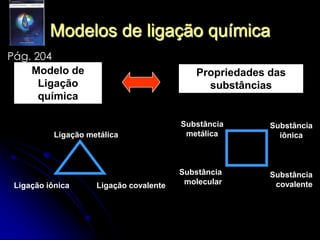
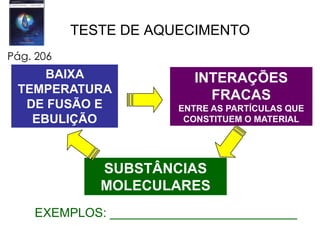
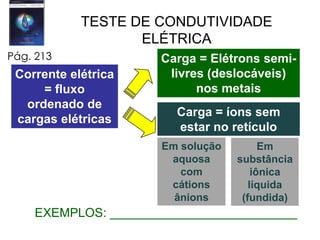
O documento lista tarefas e assuntos a serem estudados em uma próxima aula sobre ligação química iônica e metálica. Inclui exercícios sobre ligação iônica a serem feitos, propriedades periódicas dos elementos como raio atômico e iônico, energia de ionização e afinidade eletrônica que serão estudados, e tipos de substâncias e ligação química.