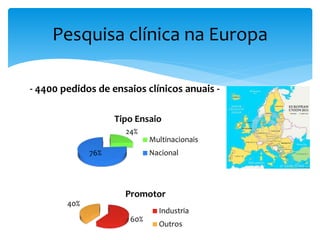
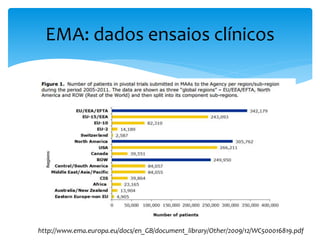
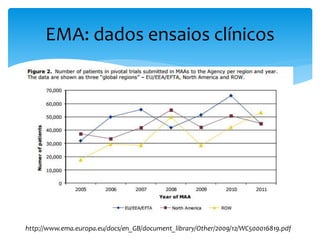
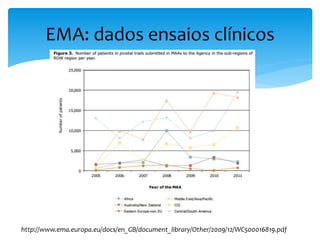
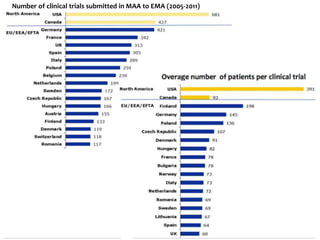
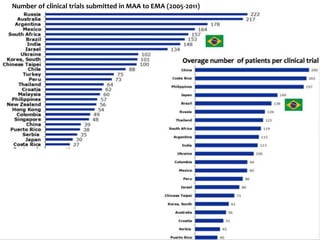
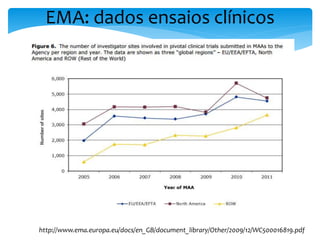
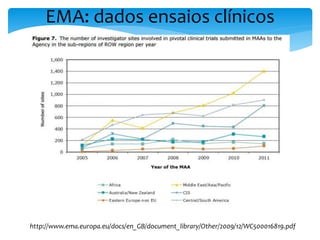
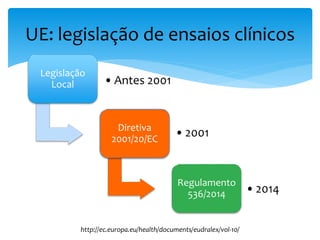
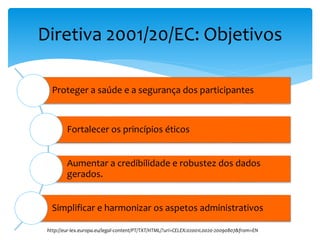
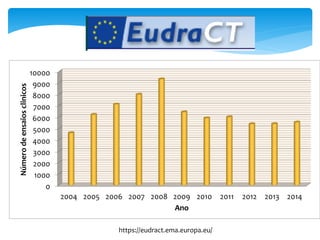
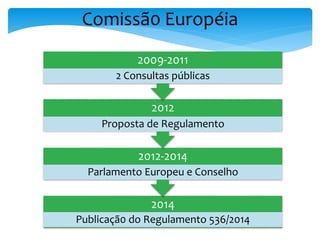
O documento aborda o regulamento europeu de ensaios clínicos, destacando as mudanças introduzidas pela regulamentação 536/2014. Os principais objetivos incluem aumentar a transparência, reduzir custos e harmonizar processos, em resposta a críticas anteriores de aumento de custos e tempo em ensaios. Além disso, o regulamento estabelece novos requisitos para a autorização de ensaios clínicos e a criação de uma base de dados pública.