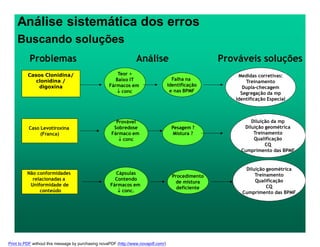
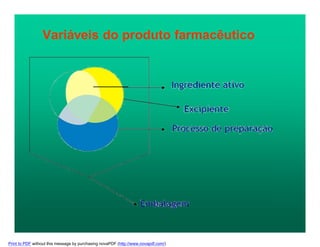
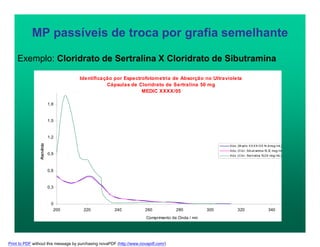
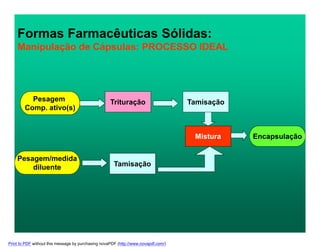
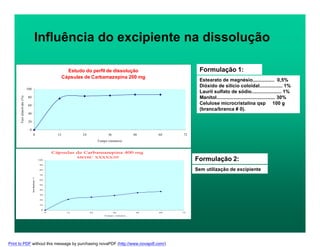
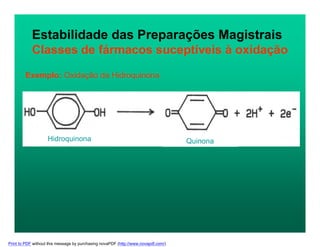
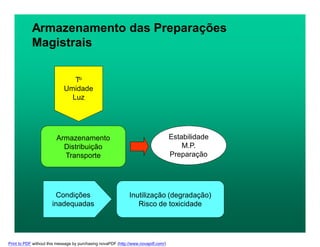
O documento discute pontos críticos na manipulação de medicamentos, focando em aspectos específicos do processo de preparo de formas farmacêuticas sólidas, como pesagem, mistura e encapsulação. Também aborda desvios de qualidade comuns e soluções, como teor inadequado de princípio ativo, heterogeneidade de conteúdo e escolha incorreta de excipientes.