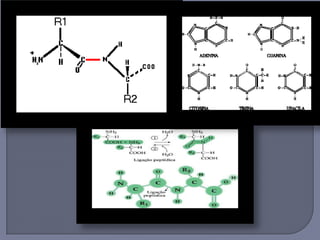
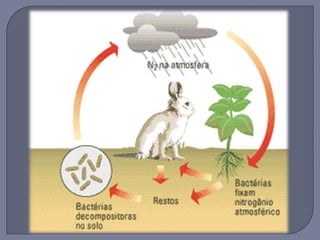
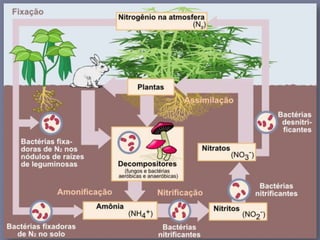
O documento descreve o ciclo do nitrogênio nos ecossistemas, incluindo suas principais formas, processos de fixação, nitrificação, desnitrificação e como é utilizado pelos seres vivos. O nitrogênio é essencial para a vida, mas em excesso pode causar eutrofização e poluição hídrica.