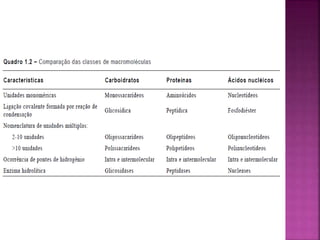
Os organismos vivos são compostos principalmente por quatro tipos de macromoléculas: proteínas, carboidratos, lipídeos e ácidos nucléicos. Estas macromoléculas são polímeros formados pela união de unidades menores através de ligações covalentes e não-covalentes, conferindo estrutura e função às células e aos organismos.