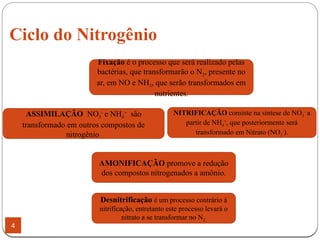
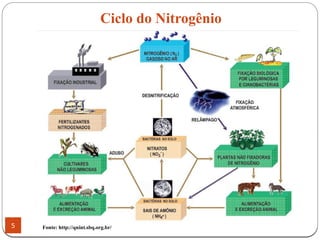
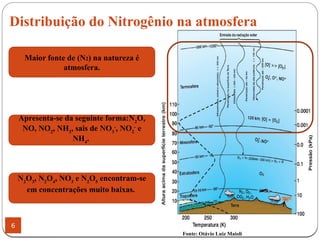
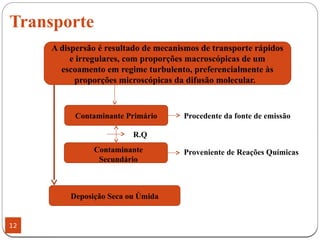
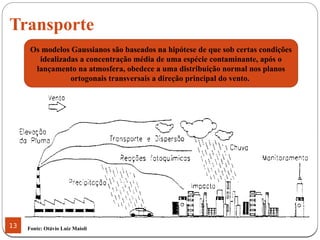
O documento discute o ciclo do nitrogênio, destacando sua importância para a vida e os processos como amonificação, nitrificação e desnitrificação. Ele também aborda a distribuição do nitrogênio na atmosfera e o impacto de poluentes nitrogenados, além de suas contribuições positivas e negativas para o meio ambiente. Além disso, menciona as reações químicas que ocorrem na atmosfera e os mecanismos de transporte de contaminantes.