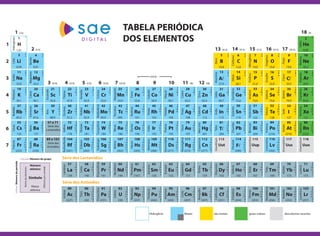
Hidrogênio à Laurêncio na Tabela Periódica
- 1. 1 (I A) 18 (0) 1 Hidrogênio 1 1 Hélio 2 2 H He 2 (II A) 13 (III A) 14 (IV A) 15 (V A) 16 (VI A) 17 (VII A) 1,01 4,00 2 Lítio 3 2 Berílio 4 2 Boro 5 2 Carbono 6 2 Nitrogênio 7 2 Oxigênio 8 2 Flúor 9 2 Neônio 10 2 1 2 3 4 5 6 7 8 Li Be B C N O F Ne 6,94 9,01 10,8 12,0 14,0 16,0 19,0 20,2 3 Sódio 11 2 Magnésio 12 2 Alumínio 13 2 Silício 14 2 Fósforo 15 2 Enxofre 16 2 Cloro 17 2 Argônio 18 2 8 8 8 8 8 8 8 8 Na 1 Mg 2 (VIII B) A 3 Si 4 P 5 S 6 C 7 Ar 8 3 (III B) 4 (IV B) 5 (V B) 6 (VI B) 7 (VII B) 8 9 10 11 (IB) 12 (IIB) 23,0 24,3 27,0 28,1 31,0 32,0 35,5 39,9 4 Potássio 19 2 Cálcio 20 2 Escândio 21 2 Titânio 22 2 Vanádio 23 2 Crômio 24 2 Manganês 25 2 Ferro 26 2 Cobalto 27 2 Níquel 28 2 Cobre 29 2 Zinco 30 2 Gálio 31 2 Germânio 32 2 Arsênio 33 2 Selênio 34 2 Bromo 35 2 Criptônio 36 2 8 8 8 8 8 8 8 8 8 8 8 8 8 8 8 8 8 8 K 8 Ca 8 Sc 9 Ti 10 V 11 Cr 13 Mn 13 Fe 14 Co 15 Ni 16 Cu 18 Zn 18 Ga 18 Ge 18 As 18 Se 18 Br 18 Kr 18 1 2 2 2 2 1 2 2 2 2 1 2 3 4 5 6 7 8 39,1 40,1 45,0 47,9 50,9 52,0 54,9 55,8 58,9 58,7 63,5 65,4 69,7 72,6 74,9 79,0 79,9 83,8 5 Rubídio 37 2 Estrôncio 38 2 Ítrio 39 2 Zircônio 40 2 Nióbio 41 2 Molibdênio 42 2 Tecnécio 43 2 Rutênio 44 2 Ródio 45 2 Paládio 46 2 Prata 47 2 Cádmio 48 2 Índio 49 2 Estanho 50 2 Antimônio 51 2 Telúrio 52 2 Iodo 53 2 Xenônio 54 2 8 8 8 8 8 8 8 8 8 8 8 8 8 8 8 8 8 8 Rb 18 Sr 18 Y 18 Zr 18 Nb 18 Mo 18 Tc 18 Ru 18 Rh 18 Pd 18 Ag 18 Cd 18 In 18 Sn 18 Sb 18 Te 18 I 18 Xe 18 8 8 9 10 12 13 14 15 16 18 18 18 18 18 18 18 18 18 1 2 2 2 1 1 1 1 1 1 2 3 4 5 6 7 8 85,5 87,6 88,9 91,2 92,9 95,9 (99) 101 103 106 108 112 115 119 122 128 127 131 6 Césio 55 2 Bário 56 2 57 a 71 Háfnio 72 2 Tântalo 73 2 Tungstênio 74 2 Rênio 75 2 Ósmio 76 2 Irídio 77 2 Platina 78 2 Ouro 79 2 Mercúrio 80 2 Tálio 81 2 Chumbo 82 2 Bismuto 83 2 Polônio 84 2 Astato 85 2 Radônio 86 2 8 8 8 8 8 8 8 8 8 8 8 8 8 8 8 8 8 Cs 18 Ba 18 Série dos Lantanídios Hf 18 Ta 18 W 18 Re 18 Os 18 Ir 18 Pt 18 Au 18 Hg 18 T 18 Pb 18 Bi 18 Po 18 At 18 Rn 18 18 18 32 32 32 32 32 32 32 32 32 32 32 32 32 32 32 8 8 10 11 12 13 14 15 17 18 18 18 18 18 18 18 18 133 1 137 2 178 2 181 2 184 2 186 2 190 2 192 2 195 1 197 1 201 2 204 3 207 4 209 5 (210) 6 (210) 7 (222) 8 7 Frâncio 87 2 Rádio 88 2 89 a 103 Rutherfórdio 104 2 Dúbnio 105 2 Seabórgio 106 2 Bóhrio 107 2 Hássio 108 2 Meitnério 109 2 Darmstadtio 110 2 Roentgênio 111 2 Copernício 112 2 Ununtrium 113 Flevório 114 2 Ununpentium 115 Livermório 116 2 Ununseptium 117 Ununoctium 118 8 8 8 8 8 8 8 8 8 8 8 8 8 Fr 18 Ra 18 Série dos Actinídios Rf 18 Db 18 Sg 18 Bh 18 Hs 18 Mt 18 Ds 18 Rg 18 Cn 18 Uut F 18 Uup Lv 18 Uus Uuo 32 32 32 32 32 32 32 32 32 32 32 32 32 18 18 32 32 32 32 32 32 32 32 32 32 32 (223) 8 (226) 8 (261) 10 (262) 11 (263) 12 (262) 13 (265) 14 (266) 15 (271) 17 (272) 18 (277) 18 (289) 18 (292) 18 1 2 2 2 2 2 2 2 1 1 2 4 6 Lantânio 57 2 Cério 58 2 Praseodímio 59 2 Neodímio 60 2 Promécio 61 2 Samário 62 2 Európio 63 2 Gadolínio 64 2 Térbio 65 2 Disprósio 66 2 Hólmio 67 2 Érbio 68 2 Túlio 69 2 Itérbio 70 2 Lutécio 71 2 8 8 8 8 8 8 8 8 8 8 8 8 8 8 8 La 18 Ce 18 Pr 18 Nd 18 Pm 18 Sm 18 Eu 18 Gd 18 Tb 18 Dy 18 Ho 18 Er 18 Tm 18 Yb 18 Lu 18 18 20 21 22 23 24 25 25 27 28 29 30 31 32 32 9 8 8 8 8 8 8 9 8 8 8 8 8 8 9 139 2 140 2 141 2 144 2 (147) 2 150 2 152 2 157 2 159 2 163 2 165 2 167 2 169 2 173 2 175 2 Série dos Lantanídios Actínio 89 2 Tório 90 2 Protactínio 91 2 Urânio 92 2 Neptúnio 93 2 Plutônio 94 2 Amerício 95 2 Cúrio 96 2 Berquélio 97 2 Califórnio 98 2 Einstênio 99 2 Fêrmio 100 2 Mendelévio 101 2 Nobélio 102 2 Laurêncio 103 2 8 8 8 8 8 8 8 8 8 8 8 8 8 8 8 Ac 18 Th 18 Pa 18 U 18 Np 18 Pu 18 Am 18 Cm 18 Bk 18 Cf 18 Es 18 Fm 18 Md 18 No 18 Lr 18 32 32 32 32 32 32 32 32 32 32 32 32 32 32 32 18 18 20 21 23 24 25 25 26 28 29 30 31 32 32 (227) 9 232 10 (231) 9 238 9 (237) 8 (242) 8 (243) 8 (247) 9 (247) 9 (251) 8 (254) 8 (253) 8 (256) 8 (253) 8 (257) 9 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 Série dos Actinídios Nome do elemento Número atômico Elétrons por camada Símbolo Massa atômica Colunas:Número do grupo Linhas: Número do período TABELA PERIÓDICA DOS ELEMENTOS Hidrogênio Metais não-metais gases nobres descobertas recentes
- 2. Partículas fundamentais do átomo Carga elétrica (uec) Massa (u) Prótons (p) +1 1 Nêutrons (n) 0 1 Elétrons (e– ) –1 1/1840 Número atômico (Z) Z = p Número de massa (A) A = p + n Átomo Íons Positivos (cátions) Negativos (ânions) p = e p > e p < e Z A p n e Isótopos = = = Isóbaros = Isótonos = Isoeletrônicos átomos ou íons com o mesmo número de elétrons Tamanhos relativos recebe elétrons Ânion A Átomo A perde elétrons Átomo B Cátion B Distribuição eletrônica (Diagrama de Pauling) 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f14 5s2 5p6 5d10 5f14 6s2 6p6 6d10 7s2 7p6 Números Quânticos Principal n (1, 2, 3,.....7) nível, distância do elétron ao núcleo. Secundário (0,1,2,...,n–1) subnível, forma do orbital. Magnético m (– a + ) orbital, orientação do orbital. Spin ms (+½ e –½) rotação do elétron. Subnível s p d f 0 1 2 3 n.º máximo de elétrons 2 6 10 14 Orbital 0 0 1 -1 0 +1 2 -2 -1 0 +1 +2 3 -3 -2 -1 0 +1 +2 +3 1 18 ns 1 2 13 14 15 16 17 ns 2 np 6 ns 2 ns 2 np 1 ns 2 np 2 ns 2 np 3 ns 2 np 4 ns 2 np 5 Elementos de transição 4s2 3d1 a 10 5s2 4d1 a 10 6s2 5d1 a 10 7s2 6d1 a 10 6s2 4f1 a 14 7s2 5f1 a 14 Elementos representativos (elétron de maior energia em subníveis s ou p) Elementos de transição externa (elétron de maior ener- gia em subníveisd) Elementos de transição interna (elétron de maior ener- gia em subníveisf) Variação das propriedades periódicas dos elementos (As setas indicam o crescimento da propriedade) Raio atômico Fr Volume atômico Rn Fr Densidade Os Ponto de fusão e ebulição W Potencial de ionização He Eletronegatividade ou caráter não-metálico e eletroafinidade Nulos F Ligações químicas Iônica Covalente Metálica Características Transferência de elétrons; atração eletrostática Compartilhamento de pares eletrônicos cátions do metal cercados por nuvem eletrônica Participantes Metal com Hidrogênio ou Ametal Ametal ou Hidrogênio com Hidrogênio ou Ametal Metal com Metal Estado físico na temperatura ambiente Sólidos Sólidos, líquidos e gases Sólidos (exceção: Hg(l) ) Condutibilidade elétrica Puros fundidos ou em solução aquosa Somente ácidos e amônia em solução aquosa Sólidos e líquidos Solubilidadeemágua Principaisexceções Solúveis Insolúveis Nitratos (NO3 – ) Acetatos (CH3 — COO– ) Ag– , Pb2+ , Hg2+ Ca2+ , Sr2+ , Ba2+ , Pb2+ Metais alcalinos, alcalinoterrosos e amônio (NH4 + ) Metais alcalinos e amônio (NH4 + ) Metais alcalinos e amônio (NH4 + ) – Sulfatos (SO4 2– ) Carbonatos (CO3 2– ) Fosfatos (PO4 3– ) Sulfetos (S2– ) Cloretos (C – ) Brometos (Br– ) Iodetos (I– )