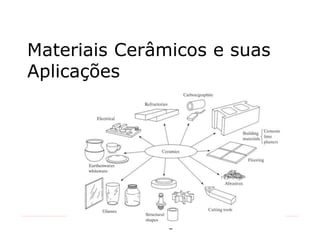
Ciências dos Materiais - Aula 12 - Materiais Cerâmicos e suas aplicações
- 1. 1 Materiais Cerâmicos e suas Aplicações
- 2. 2 • Materiais Cerâmicos: propriedades e produtos • Definição • Materiais cristalinos e amorfos • Imperfeições • Classificação dos Materiais Cerâmicos • Estrutura • Iônicos • Silicatos • Carbono • Cerâmicas de Alto Desempenho • Processos de Fabricação • Vidros • Refratários / Cimentos
- 3. 3
- 5. 5 Materiais: estrutura e propriedades Material Estrutura Propriedades Ligação Cristali- nidade Estabilidade Conduti- vidade Mecânica Cerâmico Iônica, covalente Amorfa, cristalina Alta Média Média Metálico Metálica Cristalina Média Alta Alta Polimérico Covalente, van der Waals Amorfa, semicristalina Baixa Baixa Baixa [VanVlack,1984]
- 7. 7 Estabilidade térmica e química Suscetível a corrosão, oxidaçãoMetal Resistente a corrosão, oxidação, altas temperaturas Cerâmico Degrada com solventes, altas temperaturas Polímero CaracterísticaMaterial
- 8. 8 Condutividade elétrica [Callister,2000] 10-8 a 10-7Metal 10-6 a 1018Cerâmico 108 a 1017Polímero Resistividade elétrica (ohm-m)Material
- 9. 9 Condutividade térmica [Callister,2000] 10 a 400Metal 1 a 500Cerâmico 0,01 a 0,5Polímero Condutividade térmica (W/m-K)Material
- 10. 10 Dilatação térmica depende da composição e da estrutura cristalina baixa quando comparada com metais e polímeros Possuem um número pequeno de elétrons livres condutividade elétrica é praticamente nula. existem materiais cerâmicos semicondutores, condutores e até supercondutores (para certos valores de temperatura) Condutividade térmica depende da composição e da estrutura cristalina
- 11. 11 Módulos de elasticidade 10 a 400Metal 10 a 1200Cerâmico 0,002 a 5Polímero Módulo de elasticidade (GPa)Material [Callister,2000]
- 12. 12 Resistência mecânica 100 a 2400Metal 10 a 1500Cerâmico 10 a 90Polímero Resistência sob tensão (MPa)Material [Callister,2000]
- 13. 13 Deformação 1 a 60Metal -Cerâmico 1 a 1400Polímero Deformação (%)Material [Callister,2000]
- 14. 14 Tenacidade à fratura 20 a 90Metal 0,3 a 12Cerâmico 0,5 a 6Polímero Tenacidade a fratura (MPa-m-1/2)Material [Callister,2000]
- 15. 15 DEFINIÇÃO Cerâmica vem da palavra grega keramikos (κεραμικός) que significa matéria-prima queimada. Materiais cerâmicos são compostos de elementos metálicos e não metálicos. Ligação iônico-covalente. Principalmente cristalinos (ou vítreos). Consolidados em altas temperaturas. Podem ser simples ou complexos. Podem ser óxidos, nitretos, carbetos, silicetos, aluminetos, etc.
- 16. 16 Composto Cerâmico Ponto de fusão (ºC) % Caráter Covalente % Caráter Iônico MgO 2798 27 73 Al2O3 2050 37 63 SiO2 1715 49 51 Si3N4 1900 70 30 SiC 2500 89 11 • Comparação entre a porcentagem (%) do caráter iônico e covalente de vários compostos cerâmicos; e suas respectivas temperaturas de fusão.
- 17. 17 % caráter iônico = {1- exp[-0.25(XA – XB)2]} x 100 Onde: XA e XB – eletronegatividade dos elementos
- 18. 18 Esta ampla gama de materiais inclui cerâmicas de materiais argilosos, cimento e vidros, entre outros. Até 1960, os materiais mais importantes nesta classe eram as chamadas cerâmicas clássicas, para as quais a matéria prima principal era a argila. Os produtos que são considerados cerâmicas tradicionais são porcelana branca, tijolos, vidros e cerâmicas de altas temperaturas. As cerâmicas são compostos de no mínimo dois componentes e suas estruturas cristalinas são muito mais complexas do que os metais.
- 19. 19 Cerâmica: tradicional Minerais de composição inconstante e pureza duvidosa são expostos a um tratamento térmico não-mensurável, que dura o suficiente para permitir que reações desconhecidas ocorram de modo incompleto, formando produtos heterogêneos e não- estequiométricos, conhecidos com o nome de materiais cerâmicos.
- 20. 20 Cerâmica: moderna Materiais cerâmicos são compostos sólidos formados pela aplicação de calor, algumas vezes calor e pressão, constituídos por ao menos um metal (M) e um sólido elementar não-metálico (SENM) ou um não-metal (NM), dois SENM, ou um SENM e um não-metal (NM)
- 21. 21 Metais e não-metais Metais (M): Na, Mg, Ti, Cr, Fe, Ni, Zn, Al... Não-metais (NM): N, O, H, halogênios (VII A) Sólidos elementares não-metálicos (SENM): isolantes (B, P, S, C ) ou semicondutores (Si, Ge)
- 22. 22 Tabela periódica dos elementos 19 K 20 Ca 21 Sc 22 Ti 23 V 24 Cr 25 Mn 26 Fe 27 Co 28 Ni 29 Cu 30 Zn 31 Ga 32 Ge 33 As 34 Se 35 Br 36 Kr 37 Rb 38 Sr 39 Y 40 Zr 41 Nb 42 Mo 43 Tc 44 Ru 45 Rh 46 Pd 47 Ag 48 Cd 49 In 50 Sn 51 Sb 52 Te 53 I 54 Xe 55 Cs 56 Ba * La 72 Hf 73 Ta 74 W 75 Re 76 Os 77 Ir 78 Pt 79 Au 80 Hg 81 Tl 82 Pb 83 Bi 84 Po 85 At 86 Rn 87 Fr 88 Ra ** Ac 57 La 58 Ce 59 Pr 60 Nd 61 Pm 62 Sm 63 Eu 64 Gd 65 Tb 66 Dy 67 Ho 68 Er 69 Tm 70 Yb 89 Ac 90 Th 91 Pa 92 U 93 Np 94 Pu 95 Am 96 Cm 97 Bk 98 Cf 99 Es 100 Fm 101 Md 102 No 71 Lu 103 Lw 2 He 5 B 6 C 7 N 8 O 9 F 10 Ne 13 Al 14 Si 15 P 16 S 17 Cl 18 Ar 1 H 3 Li 4 Be 11 Na 12 Mg III A II A I A IV A V A VI A VII A VIII A I B III B II B IV B V B VI B VII B VIII B Líquido GásSólido * Lantanídeos ** Actinídeos Metais Não-Metais
- 23. 23 19 K 20 Ca 21 Sc 22 Ti 23 V 24 Cr 25 Mn 26 Fe 27 Co 28 Ni 29 Cu 30 Zn 31 Ga 32 Ge 33 As 34 Se 35 Br 36 Kr 37 Rb 38 Sr 39 Y 40 Zr 41 Nb 42 Mo 43 Tc 44 Ru 45 Rh 46 Pd 47 Ag 48 Cd 49 In 50 Sn 51 Sb 52 Te 53 I 54 Xe 55 Cs 56 Ba * La 72 Hf 73 Ta 74 W 75 Re 76 Os 77 Ir 78 Pt 79 Au 80 Hg 81 Tl 82 Pb 83 Bi 84 Po 85 At 86 Rn 87 Fr 88 Ra ** Ac 57 La 58 Ce 59 Pr 60 Nd 61 Pm 62 Sm 63 Eu 64 Gd 65 Tb 66 Dy 67 Ho 68 Er 69 Tm 70 Yb 89 Ac 90 Th 91 Pa 92 U 93 Np 94 Pu 95 Am 96 Cm 97 Bk 98 Cf 99 Es 100 Fm 101 Md 102 No 71 Lu 103 Lw 2 He 5 B 6 C 7 N 8 O 9 F 10 Ne 13 Al 14 Si 15 P 16 S 17 Cl 18 Ar 1 H 3 Li 4 Be 11 Na 12 Mg III A II A I A IV A V A VI A VII A VIII A I B III B II B IV B V B VI B VII B VIII B Líquido GásSólido * Lantanídeos ** Actinídeos Tabela periódica dos elementos Sólidos Elementares Metais Não-Metálicos
- 24. 24 Exemplos de combinações M + NM: MgO, Al2O3, BaTiO3, YBa2Cu3O7... M + SENM: TiC, ZrB2... SENM + SENM: SiC, B4C SENM + NM: SiO2, Si3N4
- 25. 25 Cerâmica, vidro, argamassa Tipos Sequência de processamento Cerâmica pó forma calor Vidro pó calor forma Argamassa calor pó forma
- 26. 26 Cerâmica tradicional x avançada Cerâmica Matérias- primas Estrutura Proprie- dades Processa- mento Aplicações Tradicional (silicatos) naturais, minerais industriais (<98% pureza) não-uniforme, porosa mecânica, estética olaria, colagem, prensagem, extrusão, queima construção, produtos domésticos Avançada (alto de- sempenho, alta tecno- logia) produtos químicos industriais (>98% pureza) homogênea, menos porosa elétrica, magnética, nuclear, óptica, mecânica, térmica, química, biológica prensagem isostática, moldagem por injeção, sinterização, ligação por reação eletrônica, estrutural, química, refratários
- 27. 27 Produtos e aplicações Térmica Elétrica Magnética Óptica Nuclear Química Biológica Mecânica Estética
- 28. 28 Funções térmicas Funções Classes Aplicações Exemplos condutividade trocadores de calor para pacotes eletrônicos AlN Térmicas isolamento revestimentos isolantes para fornos de alta temperatura fibras de SiO2, Al2O3, ZrO2 refratariedade revestimentos isolantes para fornos de alta temperatura (metais fundidos, escórias) SiO2, Al2O3, ZrO2
- 29. 29
- 30. 30 Ônibus Espacial • 70% da superfície tem proteção de temperatura de 400 a 1260°C; • Placas de fibras de sílica vítrea de alta pureza (LRSI)
- 31. 31 Funções elétricas Funções Classes Aplicações Exemplos condutividade elementos de aquecimento para fornos SiC, ZrO2, MoSi2 Elétricas dielétricos capacitores BaTiO3, SrTiO3 isolamento substratos de circuitos eletrônicos Al2O3, AlN
- 32. 32 Capacitores de Cerâmica O dielétrico é um material cerâmico.
- 33. 33 Supercondutor de alta Temperatura A cerâmica YBa2Cu3O7 é um supercondutor e está sendo levitado acima de um imã permanente devido ao efeito de Meissner.
- 34. 34 Funções magnéticas Funções Classes Aplicações Exemplos magnetos duros ímãs de ferrita (Ba,Sr)O·6Fe2O3 Magnéticas e super- condutoras magnetos moles núcleos de transformadores (Zn,M)·6Fe2O3, com M=Mn,Co, Mg supercondutividade fios e magnetômetros YBa2Cu3O7
- 35. 35 Funções ópticas Funções Classes Aplicações Exemplos translucência materiais para lâmpadas de Na Al2O3, MgO Ópticas transparência cabos de fibra óptica SiO2 transparência ao infravermelho janelas para laser infravermelho CaF2, SrF2, NaCl
- 36. 36 Fios de Fibra Óptica Substitui os fios de Cu para o envio de sinais de comunicação / informação. Fios de fibras ópticas são capazes de transportar muito mais informação do que os fios de cobre convencionais. Fios de fibras ópticas são relativamente mais baratos do que os de cobre.
- 37. 37 Funções nucleares Funções Classes Aplicações Exemplos fissão combustível UO3, UC Nucleares fissão moderadores de nêutrons C fissão revestimentos em reatores Concreto
- 38. 38 Funções químicas Funções Classes Aplicações Exemplos catálise suporte de catalisador Mg2Al4Si5O15 Químicas condutividade sensitiva a gases sensores de gases ZnO, ZrO2, SnO2, Fe2O3 separação filtros SiO2, Al2O3
- 39. 39 Funções químicas sensores de gases principais materiais: ZrO2(O2) , ZnO, SnO2, Fe2O3 (H2O) alarme de vazamento de gases venenosos e hidrocarbonetos sensor de oxigênio em veículos automotores sensor de oxigênio na fabricação do aço / tratamentos térmicos
- 40. 40 Funções químicas Catalisador automotivo • 1,5 g de metais preciosos • Paládio-ródio (para veículos a gasolina) • Paládio-molibdênio (para veículos a álcool) 2CO + O2 ―> 2CO2 2C2H6 + 7O2 ―> 4CO2 + 6H2O 2NO2 + 4CO ―> N2 + 4CO2
- 41. 41 Funções biológicas Funções Classes Aplicações Exemplos biocompatibilidade cimentos CaHPO4·2H2O Biológicas biocompatibilidade próteses estruturais Al2O3
- 42. 42 Funções biológicas implantes principais materiais: Al2O3 (bioinerte) e hidroxiapatita (bioativa) ossos artificiais, dentes e juntas
- 43. 43 O osso humano contém um cerâmico que preenche 43% de sua massa – hidroxiapatita (Ca10(HPO4)6(OH)2) Alguns implantes ósseos são revestidos com hidroxiapatita para melhorar a aderência. Fonte: Schakelford
- 44. 44 Funções mecânicas Funções Classes Aplicações Exemplos dureza ferramentas de corte Al2O3, Si3N4, ZrO2, TiC Mecânicas refratariedade estrutural estatores e lâminas de turbina Al2O3, Si3N4, MgO, SiC resistência a desgaste, abrasão mancais Al2O3, Si3N4, ZrO2, SiC
- 45. 45 Funções mecânicas e térmicas ferramentas de corte principais materiais: Al2O3, TiC, TiN materiais também resistentes ao calor principais materiais: SiC, Al2O3, Si3N4 turbinas, turbo-compressores e trocadores de calor
- 46. 46 Funções estéticas Funções Classes Aplicações Exemplos cerâmica de mesa pratos, xícaras, vasos louça, porcelana Estéticas cerâmica de revestimento pisos, azulejos grés, porcelanato cerâmica sanitária vasos sanitários, pias louça, porcelana
- 47. 47 Porcelana A porcelana é um produto branco impermeável e translúcido. Ela se distingue de outros produtos cerâmicos, especialmente, da louça, pela sua vitrificação, transparência, resistência, completa isenção de porosidade e sonoridade. Matéria-prima da porcelana: argila, quartzo, caulim (minério composto de silicatos hidratados de alumínio, como a caulinita e a haloisita) e feldspato. Estes materiais são encontrados em minas, cuidadosamente lavados e purificados.
- 48. 48 Depois de secas, as peças sofrem a primeira queima, denominada biscoito, a 900 ºC, cujo objetivo é dar às peças resistências e porosidade para a perfeita absorção do verniz. Nesta etapa as peças adquirem um tom rosado. O verniz é composto pelos mesmos materiais da massa, em quantidades diferentes.
- 49. 49 Através de um processo manual de imersão, o verniz adere à superfície da peça, formando uma película de cobertura. Após a aplicação do verniz ocorre uma segunda queima, que é realizada a uma temperatura que varia entre 1380 ºC a 1400 ºC. Nesta fase a massa torna-se completamente compacta, totalmente sem porosidade, adquirindo cor branca e vitrificada (fusão do verniz sobre a massa). Esta segunda queima dura em média 31 horas, podendo chegar até 89 horas, dependendo da extensão do forno utilizado.
- 50. 50
- 51. 51 Propriedades dos Materiais Cerâmicos Estrutura cristalina ou não cristalina; Alta temperatura de fusão (até 3900°C); Todas as cerâmicas são quebradiças a temperatura ambiente; Resistência muito baixa aos esforços de tensão; Baixa resistência à fratura. Micro-fraturas são formadas facilmente sob tensão; Resistentes sob pressão. As micro-fraturas não se formam de maneira tão fácil.
- 52. 52 Propriedades dos Materiais Cerâmicos Dureza elevada e boa resistência ao atrito; Baixa tenacidade; Baixa condutividade térmica e elétrica; Alta resistência à fluência a altas temperaturas; Capacidade de se manter neutro, sem reagir, quando expostos a ambientes severos Podem ser magnetizados e desmagnetizados, alguns podem ser permanentemente magnetizados.
- 53. 53 Tensão x deformação Não é feito por um ensaio tração x deformação dificuldade no preparo de amostras com a geometria exigida dificuldade em prender materiais frágeis sem fraturá-los as falhas ocorrem com uma deformação de apenas 0,1% Realizado um ensaio de flexão transversal uma barra, com seção circular ou retangular, é flexionada até a sua fratura. Resistência à flexão
- 54. 54 • Cristais iônicos • Silicatos • Carbono Estrutura dos cerâmicos
- 55. 55 Cristais iônicos Compostos por íons eletricamente carregados ao invés de átomos. Os íons metálicos (ou cátions) estão carregados positivamente, e os íons não- metálicos (ou ânions), estão carregados negativamente. Estrutura do cristal torna-se eletricamente neutra. Estrutura dos cerâmicos
- 56. 56 Cristais Iônicos Estruturas do tipo AX Estruturas do tipo AmXn Estruturas do tipo ABmXn
- 57. 57 SILICATOS • Muitos materiais cerâmicos contêm silicatos, por serem abundantes e baratos e por possuírem propriedades importantes; • materiais de construção, como os tijolos, telhas, vidros, também são feitos de silicatos. • Os silicatos podem ser usados como, isolantes elétricos, materiais de laboratório e fibras de vidro.
- 58. 58 Unidade tetraédrica silicato Unidades tetraédricas duplas Silicatos
- 62. 62 Sílica: SiO2 Baixa densidade: Quartzo = 2.65g/cm3 Alguns polimorfos: Quartzo, cristobalita, tridimita Silicato - Sílica Si O
- 63. 63 Si O O O O 4- Silício e Oxigênio são os dois elementos mais comuns na superfície da Terra. A ligação é predominantemente covalente Os ângulos de ligação são fixos Produz uma estrutura tetraédrica Os silicatos são baseados em tetraedros Um único tetraedro (SiO4 -4) requer cátions para balancear as cargas Silicatos
- 64. 64 Dois tetraedros podem ligar-se por um único vértice: Si2O7 –6 ou pela aresta: Si2O6 –4 ou pela face: Si2O5 -2 Silicatos Si2O7 –6 Si2O6 –4 Si2O5 -2 Si Si Si O O O
- 65. 65 Os tetraedros podem formar cadeias, anéis Silicatos
- 67. 67 Grafeno
- 68. 68 Propriedades elétricas Dielétrico (isolante), Ferroelétrico (podem conduzir eletricidade, uma vez que seus domínios sejam alinhados), Piezelétricos (energia mecânica elétrica), Semicondutores (características elétricas entre os condutores e isolantes), Magnéticos.
- 69. 69 CERÂMICOS ESTRUTURAIS - ALUMINA (Al2O3) GENERALIDADES •Produzida a partir da bauxita (Al2O3.2H2O) •Existem várias formas de alumina: as mais usadas estruturalmente são a alumina alfa (hexagonal) e a gama (cúbica) Fonte: prof. Arlindo Silva - IST
- 70. 70 CERÂMICOS ESTRUTURAIS - ALUMINA (Al2O3) PROPRIEDADES •Propriedades dependem da concentração de impurezas e nível de porosidade •Porosidade pode variar desde 50% até ~0%: as qualidades estruturais variam de acordo com o percentual •Módulo de Young superior ao aço •Resistência à compressão superior a muitos aços-ferramenta •A 1000ºC preserva 50% da resistência mecânica •Grande resistência ambiental APLICAÇÕES •Usados em aplicações sem solicitações de tração/impacto, sujeitos a altas temperaturas e elevado desgaste •Pontas de foguetes, assentos de válvulas, abrasivos, etc.
- 71. 71 CERÂMICOS ESTRUTURAIS – CARBONETO DE SILÍCIO (SiC) GENERALIDADES •Usado há várias décadas, mas não como material estrutural •O carboneto de silício tipo alfa tem forma hexagonal (mais usado) e o tipo beta tem forma cúbica APLICAÇÕES •Abrasivo em pedras de esmeril e lixas de papel •Na forma de fibra é usado em compósitos como reforço •Usado como revestimento de metais e outros cerâmicos a alta temperatura, evitando a oxidação Fonte: prof. Arlindo Silva - IST
- 72. 72 CERÂMICOS ESTRUTURAIS – CARBONETO DE SILÍCIO (SiC) PROPRIEDADES •Níveis de porosidade pequenos (cerca de 3%) •Mais duro dos abrasivos tradicionais •Perde o seu poder de abrasão mais rapidamente que a alumina •Resistência e rigidez superiores à alumina •Mais leve que a alumina •Excelente resistência à oxidação a elevadas temperaturas
- 73. 73 CERÂMICOS ESTRUTURAIS – NITRETO DE SILÍCIO (Si3N4) GENERALIDADES •Desenvolvido a partir dos anos ´80 •Compete com a alumina e o SiC em ferramentas de corte Fonte: prof. Arlindo Silva - IST
- 74. 74 CERÂMICOS ESTRUTURAIS – NITRETO DE SILÍCIO (Si3N4) APLICAÇÕES •Usado em ferramentas de corte •Componentes de turbinas •Componentes de rolamentos •Componentes de motores diesel •Matrizes de extrusão a quente PROPRIEDADES •Nível de porosidade pode variar entre 20 e 0% •Mantém propriedades até 1000 ºC •Maior resistência choque térmico que maioria dos cerâmicos •1/3 da densidade do aço •Baixo coeficiente expansão térmica •Maior tenacidade que SiC e Al2O3 •Rigidez 50% superior ao aço
- 75. 75 CERÂMICOS ESTRUTURAIS – ZIRCÔNIA (ZrO2) GENERALIDADES •A zircônia parcialmente estabilizada (PSZ) é uma mistura de óxido de zircônio com magnésia, ítria, ou óxido de cálcio, para controlar transformações de fase com grande expansão volumétrica •Existem ligas de alumina-zircônia, para melhorar a resistência ao desgaste e diminuir o custo Fonte: prof. Arlindo Silva - IST
- 76. 76 APLICAÇÕES •Propriedades semelhantes ao aço fazem da PSZ um cerâmico de substituição em motores de combustão interna CERÂMICOS ESTRUTURAIS – ZIRCÔNIA (ZrO2) PROPRIEDADES •A mais importante propriedade é a elevada tenacidade à fratura •A dureza é inferior aos outros cerâmicos estruturais •Condutividade térmica reduzida •Expansão térmica e rigidez semelhantes ao aço
- 77. 77 CERÂMICOS ESTRUTURAIS – SIALON (Si3Al3O3N5) GENERALIDADES •Mistura de nitreto de silício, sílica, alumina e nitreto de alumínio •Existem duas fases dentro da mesma estrutura: uma vítrea (amorfa) e outra cristalina •Estrutura semelhante à dos vidro-cerâmicos: a fase vítrea é cristalinizada para melhorar a resistência à fluência a altas temperaturas Fonte: prof. Arlindo Silva - IST
- 78. 78 APLICAÇÕES •Aplicações que envolvam elevadas temperaturas com resistência ao desgaste e elevada resistência mecânica •Componentes de motores PROPRIEDADES •Níveis de porosidade próximos de 0% devido à fase vítrea •Propriedades mecânicas ao nível dos melhores cerâmicos •Superior resistência ao choque térmico CERÂMICOS ESTRUTURAIS – SIALON (Si3Al3O3N5)
- 79. 79 GENERALIDADES •Componentes de fibra de carbono em matriz de carbono •O processamento destes materiais é extremamente moroso e dispendioso CERÂMICOS ESTRUTURAIS – COMPÓSITOS C-C Fonte: prof. Arlindo Silva - IST
- 80. 80 APLICAÇÕES •Componentes que combinem peso reduzido e elevada resistência a altas temperaturas •Discos de freio de elevada performance (carros e aviões) •Nariz e bordos de ataque das asas do ônibus espacial PROPRIEDADES •O carbono mantém-se no estado sólido até 3600 ºC •Em contacto com o ar inflama a 600 ºC. Para isto é revestido com SiC. •Resistência específica superior às super-ligas de Níquel acima de 1200 ºC CERÂMICOS ESTRUTURAIS – COMPÓSITOS C-C
- 81. 81
- 82. 82 Técnicas de preparação de pós cerâmicos Fonte: Askeland
- 83. 83 Colagem (fundição) por Suspensão (Slip Casting) Colagem da Barbotina • Uma forma especial de gesso é feita. Este gesso é poroso e absorve a água. • Uma polpa de pó e água é preparada. Esta é denominada de suspensão (barbotina). • Esta suspensão é colocada dentro do molde. • O molde absorve a água e as partículas sólidas se depositam nas paredes do molde. • O molde é separado e o pó compactado é removido. • O pó compactado é sinterizado. • O slip casting permite trabalhar com formas complexas.
- 84. 84 Fundição por Suspensão Colagem da Barbotina (Slip Casting) Enchimento do molde Compactação Retirar excesso Extração do molde Fonte: Askeland
- 85. 85 Fundição por Suspensão Bule de chá sendo removido do molde após Colagem da Barbotina.
- 86. 86 Produção de Louça Sanitária
- 87. 87 Sinterização • O pó cerâmico é misturado com um ligante ou lubrificante, após é pressionado dentro de um molde com a forma desejada. • O pó compactado é removido do molde e aquecido a altas temperaturas onde as partículas coalescem ou sinterizam entre si na forma de um objeto sólido. • A sinterização ocorre pelo movimento dos átomos no sólido chamado de difusão, causando geralmente uma diminuição da porosidade e contração na peça.
- 88. 88 Sinterização de cerâmicos As partículas se ligam através de pontos de contato. Grande números de poros. Formação de pescoço entre as partículas, o que torna a peça mais densa. Final: poros arredondados com menor espaço entre eles.
- 89. 89 Microestrutura de um cerâmico após sinterização
- 90. 90 Processamento de Pó Compressão Uniaxial Compressão Isostática Moldagem por Injeção de Pós (Powder Injection Moulding - PIM)
- 91. 91 Compressão Uniaxial Compressão Isostática
- 93. 93 Sinterização por Reação (Reaction Bonding) Nitreto de silício é feito por um processo chamado de reação de ligação. O pó de silício é moldado na forma desejada. Ele reage então a altas temperaturas com gás de nitrogênio para formar o nitreto de silício.
- 94. 94
- 95. 95 Colagem em fita Produção de filmes finos sinterizados; Circuitos microeletrônicos - substrato de alumina; Capacitores de titanato de bário.
- 96. 96 Representação do processo de fundição em fita.
- 97. 97 Vidros • Vasilhames • Janelas • Lentes • Fibra de vidro • Os vidros comerciais mais fabricados são os soda cal, que são combinações de sílica + cal + soda • Principal óxido: SiO2 ; outros óxidos: CaO, Na2O, K2O e Al2O3. • Os cristais são produzidos à base de sílica, K2O, Na2O mais um percentual de óxido de chumbo (até 30% de PbO), o que garante o brilho metálico.
- 98. 98 Vidros Vidro-formadores: B2O3; SiO3; GeO2; P2O5; V2O5; As2O3 (óxidos ácidos) – formadores de rede; Intermediários: Al2O3; Sb2O3; ZrO2; TiO2; PbO; BeO; ZnO (anfóteros) – não formam vidros sozinhos, mas em combinação com os primeiros adquirem o papel de formador de rede; Modificadores: MgO; Li2O; BaO; CaO; SrO; Na2O; K2O (óxidos básicos) – similar aos 2º, mas de outra classe, formam ou modificam a rede.
- 99. 99 Acessórios: por vezes usados em pequenas quantidades, como corantes, refino, eliminação de bolhas, opalinos, etc. FeO: cor verde azulada; Fe2O3: cor verde amarelada; Co2O3: cor azul; CuO: cor azul esverdeada; Cr2O3: cor verde.
- 100. 100 Tipos principais Vidro alcalino (comum : > 95%); Vidro chumbo (cristal); Vidro boro-silicato (vidrarias e utensílios domésticos); Fibra de vidro; Vidro opalino (opalescente); Vidro para termômetro (melhor controle de espessura); vidro de sílica (100% SiO2); Vidro oftálmico (fabricação de lentes).
- 101. 101 Os produtos de vidro são conformados (moldados) a quente. Quando o material está “fundido” apresentando-se como um material de elevada viscosidade, ele pode ser deformado plasticamente sem se romper).
- 102. 102
- 103. 103 Conformação de vidros [Norton,1952:162;Fernandes,1999:62] Prensagem pratos Sopro garrafas Laminação ou estiramento vidro plano Fiação fios, fibras
- 104. 104 ©2003 Brooks/Cole, a division of Thomson Learning, Inc. Técnicas de fabricação de vidros planos. Vidros planos Fonte: Askeland
- 105. 105 ©2003 Brooks/Cole, a division of Thomson Learning, Inc. Processos de fabricação de produtos de vidro: (a) prensagem; (b) prensagem e sopro; (c) trefilação. Fonte: Askeland
- 109. 109 Fios e tubos [Norton,1952:167;Schaffer,1999:689] Platina Fibra de vidro Vidro fundido Vidro fundido Mandril Fluxo de ar Tubo Fiação Fabricação de tubos
- 110. 110 ©2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning™ is a trademark used herein under license. Efeito do Na20 no reticulado do vidro de sílica. O óxido de sódio modifica o reticulado vítreo ao romper as ligações atômicas e reduzir a estabilidade do vidro. Fonte: Askeland
- 111. 111 Tratamento térmico de vidros [Callister,1996:417] Recozimento (annealing) Aquecimento a temperatura de recozimento, seguida de resfriamento Alívio de tensões térmicas Têmpera (quenching) Aquecimento a T>Tg e < ponto de amolecimento Resfriado a T ambiente com jato de ar ou banho de óleo Tensões residuais compressivas na superfície e de tração no interior
- 112. 112 Propriedades dos vidros Não ocorre a cristalização (ordenação dos íons em uma estrutura cristalina) durante o resfriamento; Quando o líquido é resfriado, aumenta a sua viscosidade (e diminui o seu volume) até que a viscosidade aumente tanto que o material comece a apresentar o comportamento mecânico de um sólido; Não existe uma temperatura de fusão cristalina, mas uma temperatura de transição vítrea (Tg).
- 113. 113 Propriedades dos vidros Volumeespecífico (vol/massa) Temperatura Tg sólido amorfo Tm líquido cristalização sólido cristalino líquido super resfriado Tg temperatura de transição vítrea Tm temperatura de fusão cristalina
- 114. 114 ©2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning™ is a trademark used herein under license. Vidro resfriado rapidamente para produzir tensões compressivas na superfície. Fonte: Askeland
- 115. 115 Devitrificação e vitrocerâmica [Barsoum,1997:323] Temperatura Tempo Crescimento Nucleação Fusão e conformação
- 116. 116 Abrasivos Elementos de moagem, polimento e de corte Tipos de abrasivos: • Diamantes • Carbeto de silício • Carbeto de alumínio • Óxido de alumínio • Carbeto de tungstênio
- 117. 117 Produtos de Argila • Produtos estruturais (Tijolos, telhas, tubulações, etc.) • Produtos brancos (Porcelana, louça, etc.). Este produtos são compostos de: Alumina (Al2O3) + Sílica (SiO2) Refratários • Refratários para fornos • Equipamentos de tratamento térmico • Equipamentos de geração de energia Tipos de refratários: • Neutros – cromita • Ácidos – sílico-aluminoso • Básicos – magnesíticos • Refratários especiais (zirconita, magnesita, alumina, SiC). Usados como resistência elétrica, material de moagem, componentes internos de fornos.
- 118. 118 MATERIAIS REFRATÁRIOS DEFINIÇÃO: - Materiais de construção que têm que resistir a altas temperaturas e manter suas propriedades físicas e químicas nas condições de serviço. - Materiais não-metálicos, inorgânicos, de ligação iônico-covalente, geralmente cristalinos.
- 119. 119 MATERIAIS REFRATÁRIOS -não existe material, a pressão normal, sólido > 4.000oC C ~3.700oC HfC ~3.890oC HfC.4TaC ~3.940oC - maior parte dos materiais refratários constituída de SiO2, Al2O3, CaO e MgO, C, carbonetos, boretos e nitretos SiO2 ~1.726oC Al2O3 ~2.054oC 3Al2O3.2SiO2 ~1.828oC MgO ~2.800oC MgO.Al2O3 ~2.135oC Cr2O3 ~2.400oC $ CaO ~2.570oC hidrata ZrO2 ~2.700oC instável BeO ~2.600oC tóxico ThO2 ~3.000oC radioativo - no entanto: 98MgO + 0,8 CaO + 0,4 SiO2 + 0,6 (Al2O3+Fe2O3) + 0,2 B2O3 ~ 1.000oC !
- 120. 120 MATERIAIS REFRATÁRIOS CONDIÇÕES DE SERVIÇO (aplicações): alta temperatura, esforços mecânicos, vibrações, choque térmico, desgaste físico, corrosão química - associadas à produção do aço e metais não ferrosos, vidro, cerâmica e outros processos (indústria petroquímica, incineradores industriais, etc.)
- 121. 121 MATERIAIS REFRATÁRIOS CLASSIFICAÇÃO: CRITÉRIOS: -matéria-prima: argilosos e não-argilosos -composição química: alta-alumina, magnesíticos -natureza química: básicos (MgO), ácidos (SiO2), neutros muito usada na metalurgia: -escórias básicas atacam refratários ácidos e vice-versa -neutros: imune aos dois tipos de escórias(cromita, forsterita e carbono) -forma: monolíticos, formatados (peças prontas) -utilização: isolantes térmicos
- 122. 122 MATERIAIS REFRATÁRIOS CLASSIFICAÇÃO: ÁCIDOS (de sílica) -da série sílica-alumina silicosos ou de meia sílica argilosos ou de chamote (rejeitos) mulíticos de silimanita, andaluzita e cianita sintéticos -da série alta-alumina de bauxita, sinterizados de coríndon eletrofundidos BÁSICOS -magnesíticos ou de magnésia -crómia-magnésia ou cromo-magnesianos -dolomíticos
- 123. 123 MATERIAIS REFRATÁRIOS CLASSIFICAÇÃO: NEUTROS -cromítico ou de cromita -forsteríticos (forsterita, olivina) ELETROFUNDIDOS -mulíticos -alumina-zircônia-sílica -magnésia-crômia NÃO-MOLDADOS -argamassas refratárias (materiais de ligação) -misturas para construção monolítica massas plásticas (pega química ou químico-cerâmica) concretos refratários (pega hidráulica) -misturas projetáveis (para reparações)
- 124. 124 MATERIAIS REFRATÁRIOS MATÉRIA-PRIMA: mais comum: natural óxidos de metais simples, duplos, triplos carbono, grafite, carbeto de silício novos materiais: carbetos, nitretos, boretos, silicetos para aplicações mais sofisticadas sintéticos, alta pureza, e propriedades sob controle
- 125. 125 MATERIAIS REFRATÁRIOS FORMA: -2/3 peças formatadas -1/3 não formatado (monolíticos, projetados ou socados)
- 126. 126 MATERIAIS REFRATÁRIOS TIPOS E APLICAÇÕES - em função da matéria-prima: argilosos e não-argilosos mais comuns: SiO2, Al2O3, MgO, CaO, ZrO2 ácidos: SiO2, ZrO2, básicos: MgO, CaO, Cr2O3 neutros: FeO.Cr2O3, 2MgO.SiO2, Al2O3
- 127. 127 MATERIAIS REFRATÁRIOS -Alumina extra-alta: bauxita ou alumina (fundida ou densamente sinterizada) 87,5% de Al2O3. Refratariedade ~1815oC -Mullita: 3Al2O3.SiO2 cianita, silimanita e andalusita, bauxita ou misturas de silicatos de alumínio. É o silicato mais estável -Sílica: Contaminantes: alumina e álcalis. Semi-sílica -Carbeto de silício: Reação entre areia e coque em um forno elétrico -Zirconita: ZrO2.SiO2 = estabilização CaO, MgO, Y2O3
- 128. 128 MATERIAIS REFRATÁRIOS MASSAS REFRATÁRIAS: VANTAGENS Matéria-prima: - a mesma matéria-prima que a usada em materiais formatados Preparo: - simples e rápido Propriedades: - melhor resistência ao choque-térmico - maior capacidade de isolamento Construção: - não há juntas - compatibilidade com a maioria dos fornos - de colocação mais simples Econômica: - não há as etapas de conformação e queima - preenchimento de qualquer geometria - menor custo de transporte - mais rápida entrega
- 129. 129 MATERIAIS REFRATÁRIOS MASSAS REFRATÁRIAS: DESVANTAGENS Matéria-prima: - custo do cimento para alguns concretos refratários mais elevados - alguma degradação quando em deposição prolongada - perigo de sedimentação de componentes - cuidados no preparo (quantidade de água e aditivos) Propriedades: - alta porosidade - pequena resistência à erosão por escórias - menor resistência quando não há uma sinterização homogênea e efetiva - rachaduras
- 130. 130 Cimentos Produtos argilosos que endurecem com reação com água; Cimento Portland, gesso de Paris, cal, fosfato de alumínio; Concreto comum: agregado graúdo, agregado miúdo, cimento e água; Concreto especial: reforçado com fibra de vidro (GRC).
- 131. 131 Cimento Portland Componentes: cal, sílica, alumina e óxido de ferro Cozimento – fusão parcial – a 1450C – chamado clínquer, ao qual é adicionado gesso (para início de pega). Tipos de cimento: cimento Portland, cimento Portland branco, cimento aluminoso, cimento de pega rápida, cimento metalúrgico. Tipos de uso: pasta, argamassa, concreto.
- 132. 132 Outras aplicações Revestimentos: esmalte cerâmico; Filmes finos: tarja de cartão magnético (óxido de ferro), telas sensíveis ao toque (óxido de estanho e índio); Fibras: usadas em diferentes compósitos.
- 133. 133 PEI (Porcelain Enamel Institute / Instituto da Porcelana Esmaltada): é um índice usado como norma internacional para indicar a resistência do esmalte da cerâmica ao desgaste quando submetido à ação de sujeiras abrasivas em função do uso.
- 134. 134
- 135. 135 • Materiais Cerâmicos: propriedades e produtos • Definição • Materiais cristalinos e amorfos • Imperfeições • Classificação dos Materiais Cerâmicos • Estrutura (cristalinos) • Iônicos • Silicatos • Carbono • Cerâmicas de Alto Desempenho • Processos de Fabricação • Vidros (amorfos) • Refratários / Cimentos
- 136. 136