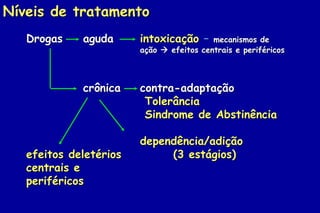
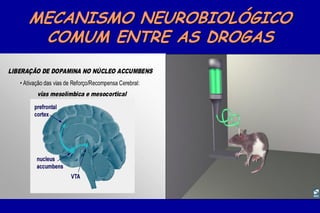
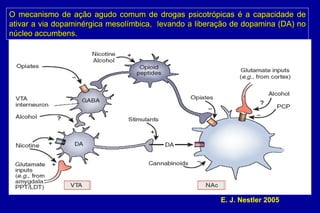
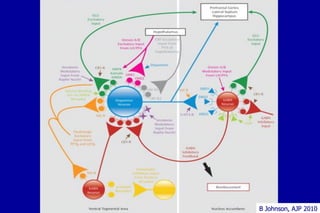
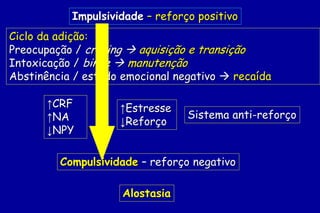
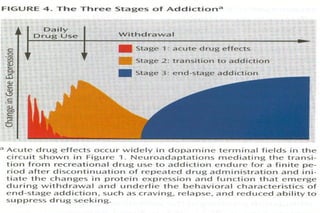
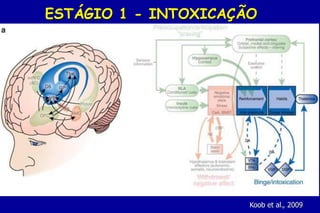
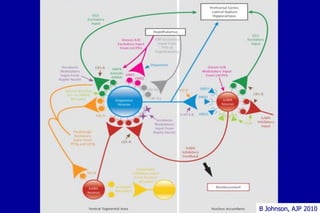
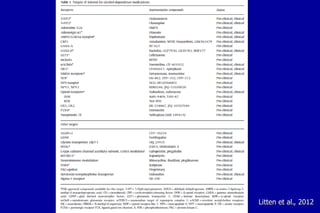
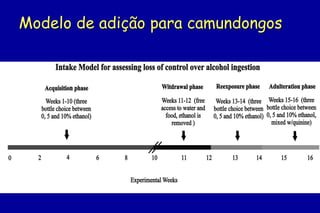
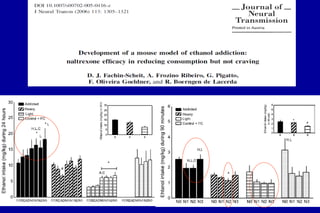
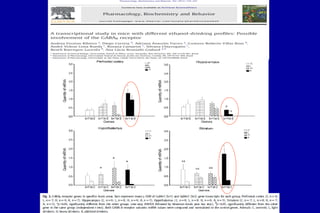
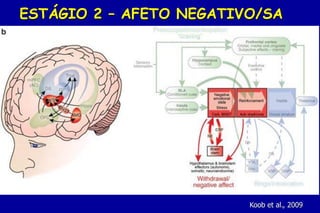
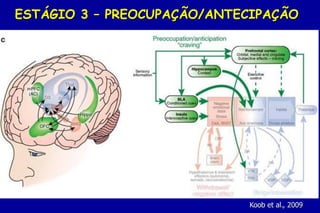
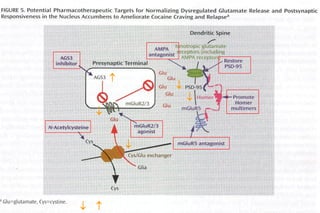
O documento discute a neurobiologia da adição a substâncias psicoativas. Resume que o uso crônico de drogas causa adaptações neuroplásticas que levam à dependência, incluindo a liberação excessiva de dopamina no núcleo accumbens e mudanças nos circuitos de recompensa do cérebro que fortalecem associações entre estímulos e consumo de drogas.