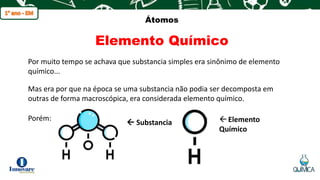
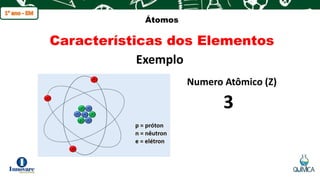
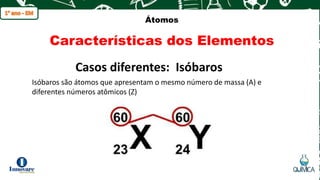
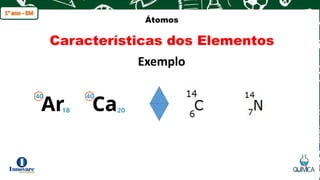
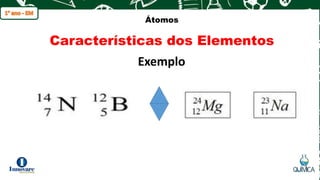
O documento apresenta os principais modelos atômicos propostos por Dalton, Thomson, Rutherford e Bohr. Também descreve as partículas que compõem o átomo (próton, nêutron e elétron), conceitos de elemento químico, número atômico, número de massa e características de isótopos, isóbaros e isótonos.