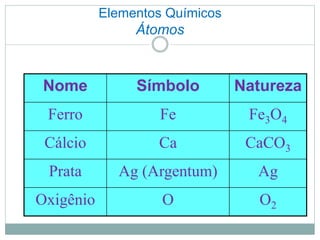
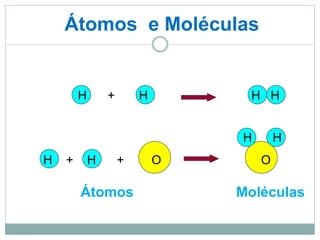
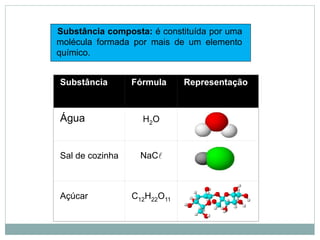
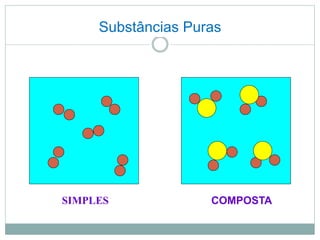
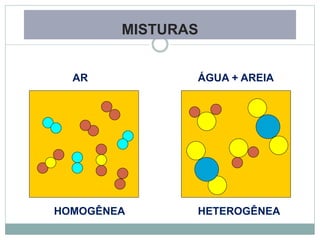
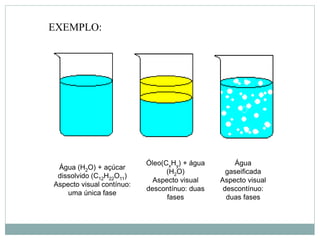
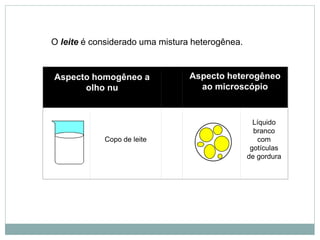
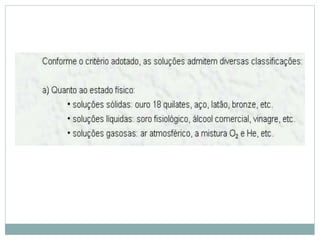
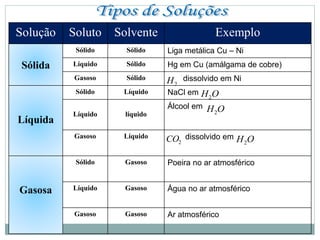
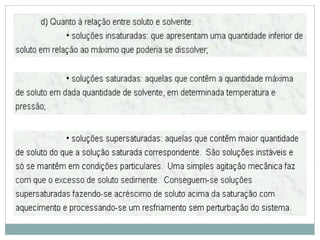
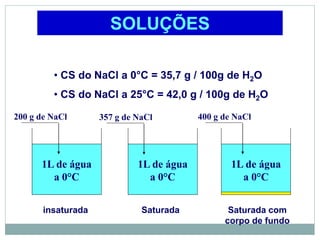
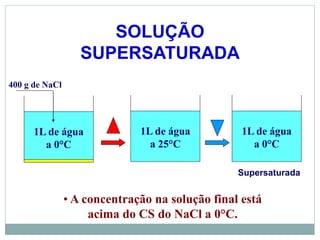
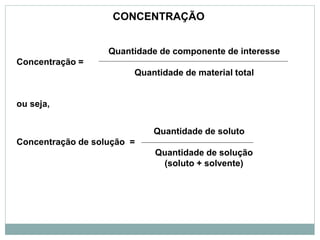
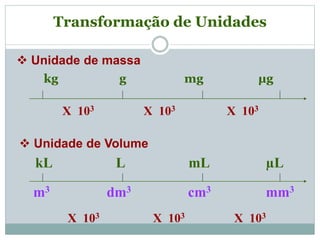
O documento descreve conceitos básicos de química como átomos, moléculas, elementos, substâncias puras e misturas. Explica que a matéria é constituída por átomos que formam moléculas, e que existem substâncias simples e compostas. Apresenta também os conceitos de solução, concentração e diluição de soluções.