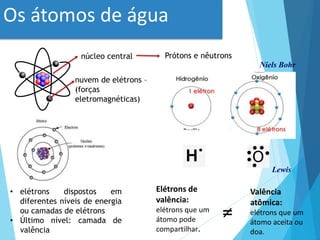
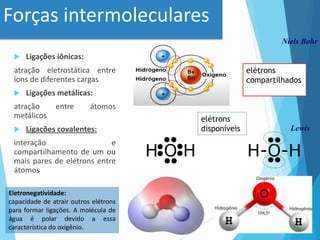
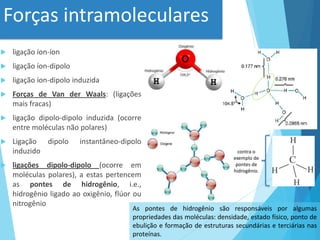
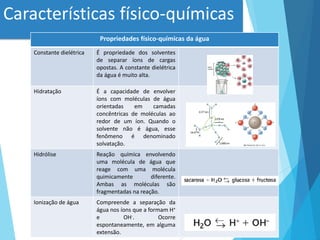
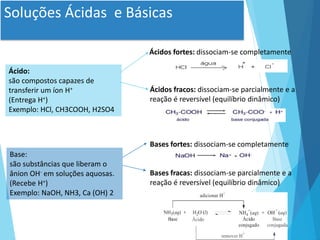
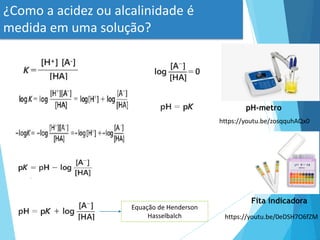
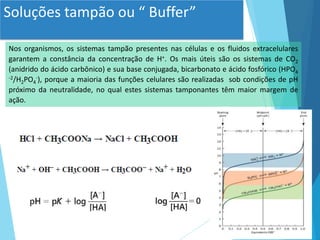
Este documento discute conceitos fundamentais sobre água, pH e sistemas tampão. Ele explica que a água é o solvente universal na natureza e discute suas propriedades físico-químicas importantes, como sua capacidade de formar pontes de hidrogênio. Também define conceitos-chave como ácidos, bases, pH e sistemas tampão, explicando como esses sistemas ajudam a manter o pH constante em organismos vivos.