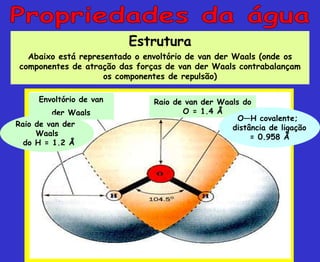
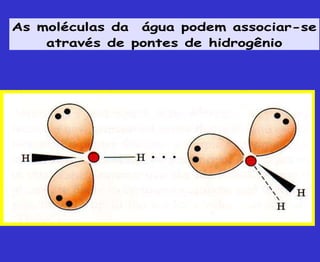
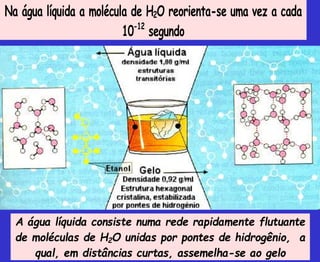
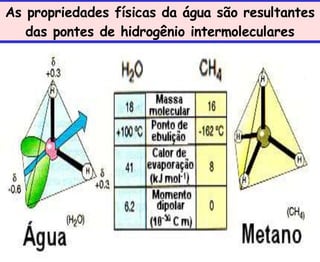
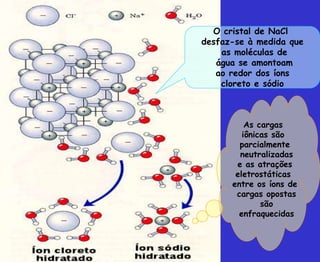
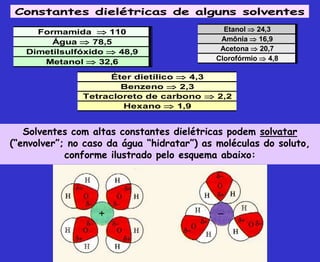
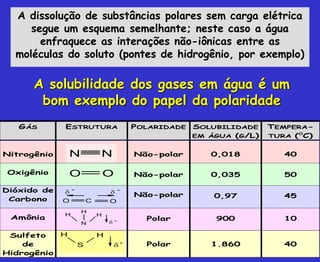
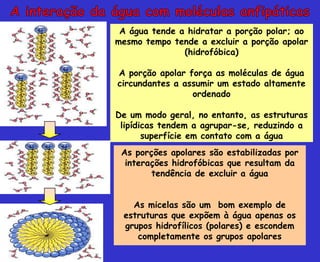
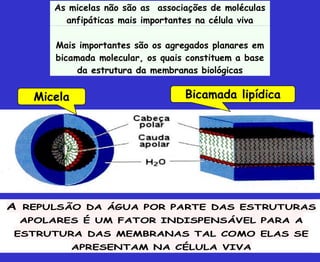
O documento discute os principais conceitos da bioquímica, incluindo: 1) A bioquímica estuda as reações químicas que ocorrem nos seres vivos; 2) As biomoléculas fundamentais incluem proteínas, carboidratos, lipídeos e ácidos nucleicos; 3) A água é essencial para a vida e permite a estrutura e função das biomoléculas através de suas propriedades como solvente e formação de pontes de hidrogênio.






![Em soluções aquosas diluídas o valor de [H2O] é
essencialmente constante e igual a 1000 g litro-1
ou seja
1000 g litro-1
/18,015 g mol–1
= 55,5 M; por isto, pode-se
incluir [H2O] na constante K, definindo uma nova constante Ka
Pode-se analisar a dissociação da água da mesma maneira:
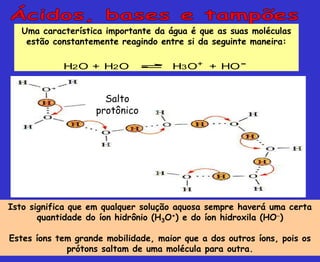
H2O + H2O H3O+ + HO-
Ou, na forma abreviada
H2O H + HO
+ -
A expressão de equilíbrio:
]
O
H
[
]
OH
][
H
[
K
2
](https://image.slidesharecdn.com/bioquimica1aguaphesolucoestampao-240412174350-1fac2e31/85/bioquimica_1_agua_pH_e_solucoes_tampao-ppt-17-320.jpg)
![Como [H2O] é constante e igual a 55,5 M, pode-se
definir uma nova constante Kw (constante de ionização
da água):
]
OH
][
H
[
]
O
H
[
K
K 2
w
A 25o
C Kw é igual a 1014
M2
Na água pura
M
10
K
]
HO
[
]
H
[ 7
w
[H+
] > 107
M solução ácida
(neste caso HO
< 107
M)
[H+
] < 107
M solução básica ou alcalina
(neste caso HO
> 107
M)
Nos líquidos biológicos o valor de [H+
] costuma estar
próximo de 107
M; no sangue, por exemplo [H+
] = 4,0
108
M
Há exceções, no entanto, como o suco gástrico, por
exemplo.](https://image.slidesharecdn.com/bioquimica1aguaphesolucoestampao-240412174350-1fac2e31/85/bioquimica_1_agua_pH_e_solucoes_tampao-ppt-18-320.jpg)
![Tomando logaritmos negativos da expressão do
produto iônico da água (Kw = [H+
][HO–
]), teremos
])
OH
][
H
log([
)
10
log(
K
log 14
w
Se chamarmos –log[H+
] = pH e –log[HO–
] =
pOH, podemos escrever:
pOH
pH
14
A escala de pH é prática e costuma ser usada entre 0 e 14
Na água pura
pH = log[H+] = log(107)= 7
Também na água pura:
pOH = 14 – pH = 14 – 7 = 7
]
OH
log[
]
H
log[
](https://image.slidesharecdn.com/bioquimica1aguaphesolucoestampao-240412174350-1fac2e31/85/bioquimica_1_agua_pH_e_solucoes_tampao-ppt-19-320.jpg)
![Numa solução 1 M de
HCl, um ácido forte
que dissocia quase
100%
HCl H+ + Cl
pH = –log[H+] = –
log(1) = 0
Numa solução 1 M de
NaOH, que também
dissocia 100%
NaOH HO + Na+
pOH = –log[HO] = –
log(1) = 0
pH = 14 – pOH = 14
– 0 = 14
Progressi-
vamente
mais básico
Progressi-
vamente
mais ácido
Neutro
14
13
12
11
10
9
8
7
6
5
4
3
2
1
0
NaOH 1 M
HCl 1 M
Suco de tomate
Alvejante
doméstico
Detergente
amoniacal
Suspensão de
fermento químico
Clara de ovos
Sangue humano
Lágrimas
Leite, saliva
Café preto
Cerveja
Vinho tinto
Refrigerante
vinagre
Suco de limão
Suco gástrico](https://image.slidesharecdn.com/bioquimica1aguaphesolucoestampao-240412174350-1fac2e31/85/bioquimica_1_agua_pH_e_solucoes_tampao-ppt-20-320.jpg)
![Na célula predominam ácidos e bases fracos
A relação entre o pH e o grau de dissociação de um ácido
ou base fraco pode ser melhor analisada em termos da
equação de Henderson-Hasselbalch
Consideremos novamente a equação simplificada da
dissociação de um ácido fraco em solução aquosa
HA H + A
+ -
A expressão de equilíbrio:
]
HA
[
]
A
][
H
[
Ka
]
A
[
]
HA
[
K
]
H
[ a
Tomando
logaritmos
negativos
]
A
[
]
HA
[
log
K
log
]
H
log[ a
Como –log[H+
] = pH, se definirmos –log Ka = pKa podemos
escrever
]
HA
[
]
A
[
log
pK
pH a
ou, rearranjando](https://image.slidesharecdn.com/bioquimica1aguaphesolucoestampao-240412174350-1fac2e31/85/bioquimica_1_agua_pH_e_solucoes_tampao-ppt-21-320.jpg)

![Em termos gerais:
desde que a razão ]
prótons
de
doador
[
]
prótons
de
aceptor
[
seja conhecida,
pode-se calcular o pH de qualquer solução
O valor de pKa é uma medida da força de um ácido
QUANTO MENOR O VALOR pKa, MAIS FORTE É O ÁCIDO
Costuma-se usar o valor de pKa também para medir a força
de bases fracas; para tanto utiliza-se o pKa do ácido
conjugado
Portanto, vale a regra
QUANDO MAIOR O pKa DE SEU ÁCIDO CONJUGADO, MAIS
FORTE É A BASE
E TAMBÉM, QUANDO MENOR O pKb, MAIS FORTE É A BASE
14
pK
pK b
a
](https://image.slidesharecdn.com/bioquimica1aguaphesolucoestampao-240412174350-1fac2e31/85/bioquimica_1_agua_pH_e_solucoes_tampao-ppt-23-320.jpg)

![
x
c
x
log
pK
pH
o
a
onde x são os equivalentes
de HO
adicionados e co os
equivalentes de HA
inicialmente presentes
Nas extremidades das curvas o pH varia MUITO com POUCOS
equivalentes de HO
adicionados
Na faixa média, com pH’s próximos aos dos pKa’s, no entanto, o pH
varia POUCO com MUITOS equivalentes de HO
adicionados
A faixa que resiste a variações de pH é chamada de faixa
tamponante; ela situa-se mais ou menos, entre pKa 1 e pKa + 1
No ponto inicial existe
apenas HA; à medida que
HO é adicionado forma-se
A
No ponto médio pH = pKa e
[HA] = [A]
No ponto final existe
apenas A
Durante a maior parte da
curva, exceto nas
extremidades, vale a
equação
H
NH
NH 3
4
H
HPO
PO
H 2
4
4
2
H
COO
CH
COOH
CH 3
3](https://image.slidesharecdn.com/bioquimica1aguaphesolucoestampao-240412174350-1fac2e31/85/bioquimica_1_agua_pH_e_solucoes_tampao-ppt-25-320.jpg)