Incorporar apresentação
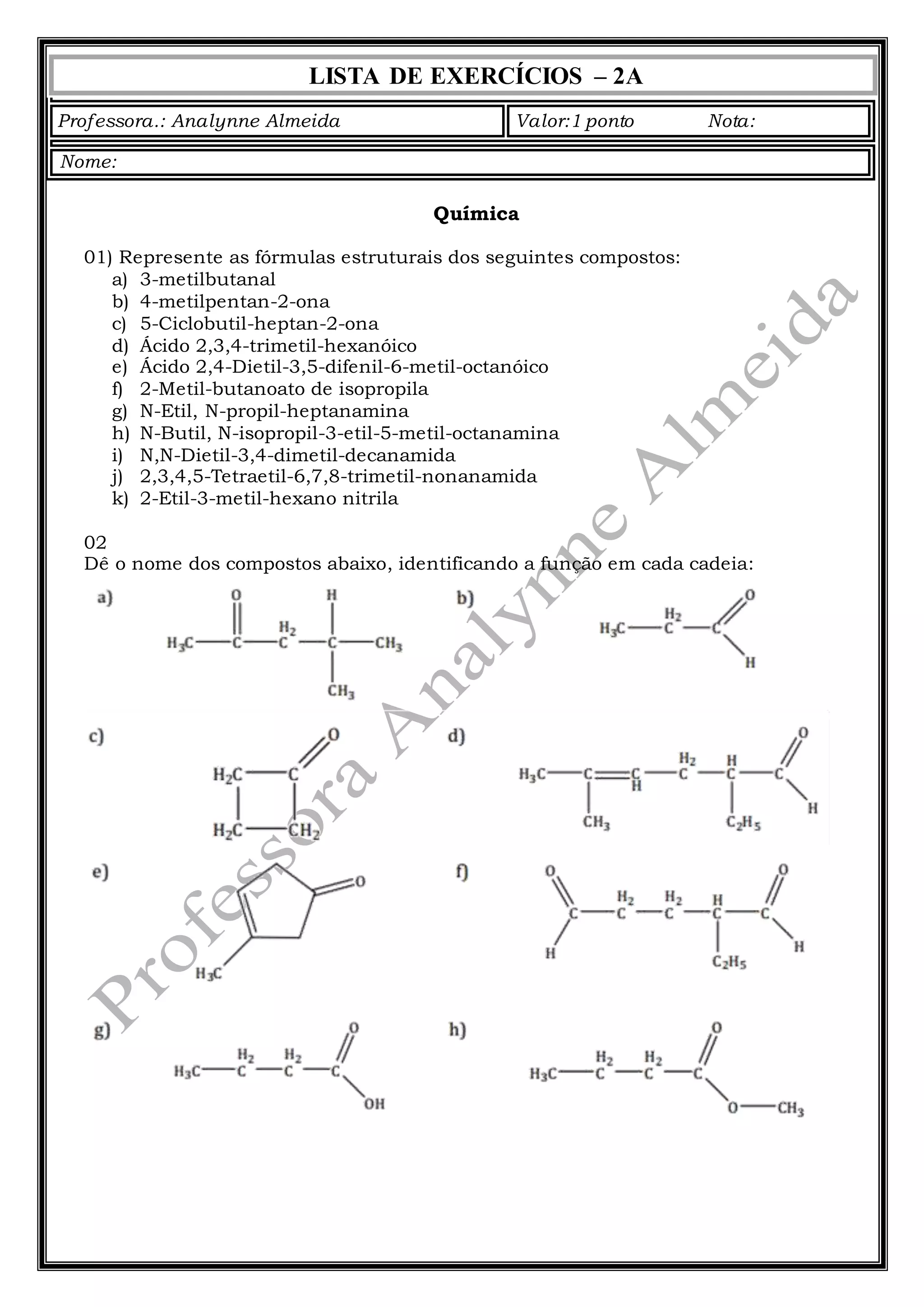
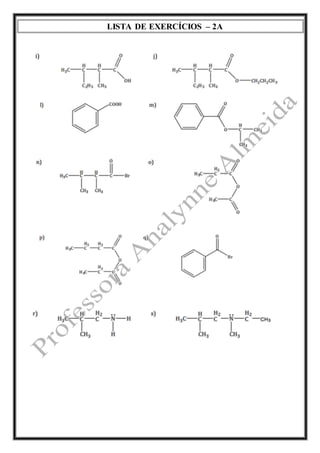
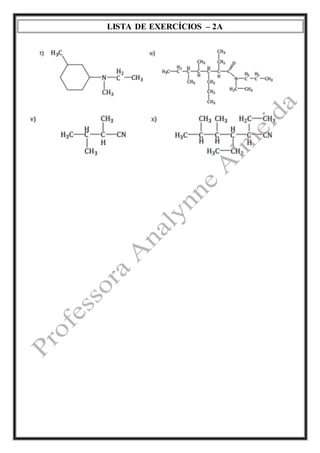

A lista de exercícios pede para (1) representar as fórmulas estruturais de vários compostos orgânicos e (2) nomear compostos identificando suas funções. Os exercícios incluem aldeídos, cetonas, ácidos carboxílicos, ésteres, aminas e nitrilas.


