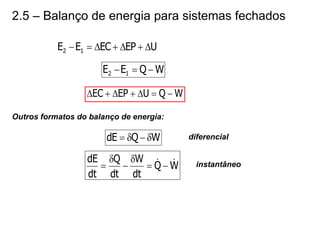
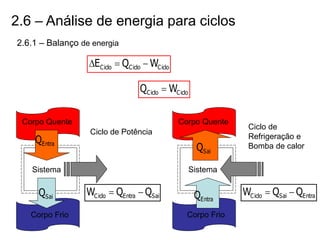
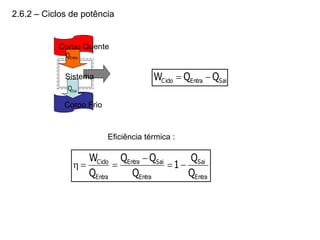
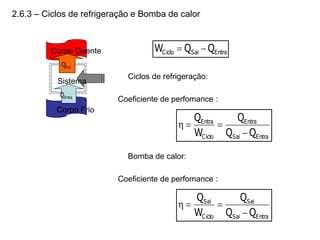
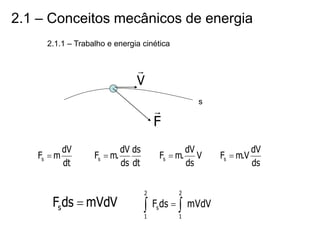
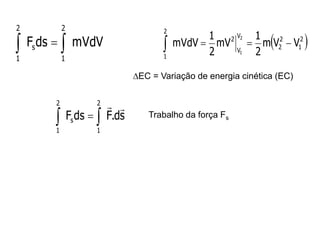
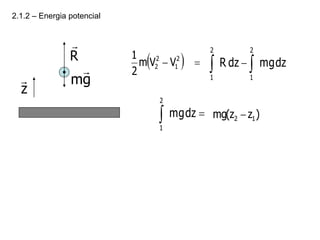
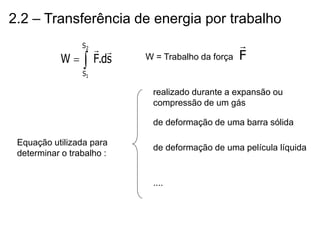
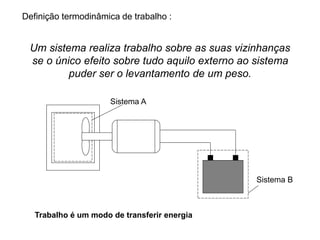
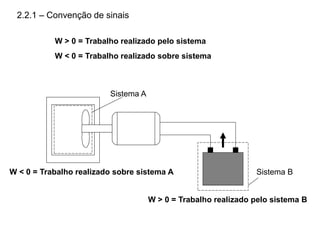
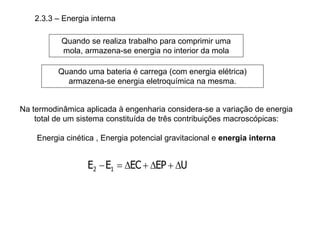
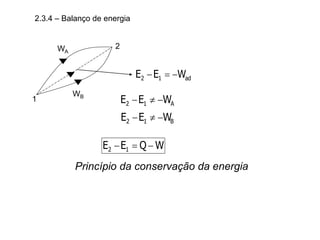
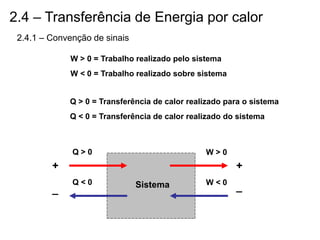
O capítulo descreve conceitos de energia mecânica e termodinâmica. Apresenta as definições de trabalho, energia cinética e potencial. Estabelece a primeira lei da termodinâmica, que relaciona a variação de energia de um sistema à quantidade de trabalho e calor transferidos. Por fim, discute análise energética para processos cíclicos.




![
2
1
Q
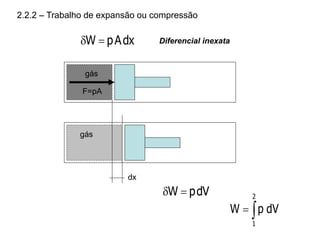
Q Diferencial inexata
Transferência de calor não é uma propriedade do sistema !
Taxa de transferência de calor:
dt
Q
Q
2
1
t
t
dt
Q
Q
(Potência térmica) [J/s] ou [W]
A
dA
q
Q
q
= fluxo de calor [W/m2]](https://image.slidesharecdn.com/captulo2-energia-230924001138-56f93dce/85/Cap_tulo-2-Energia-ppt-16-320.jpg)