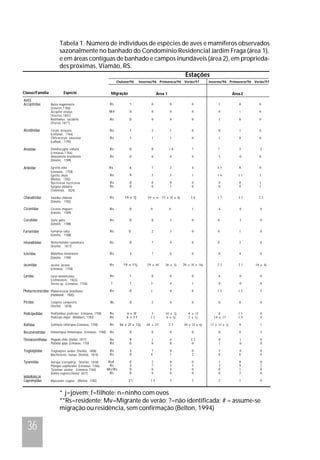
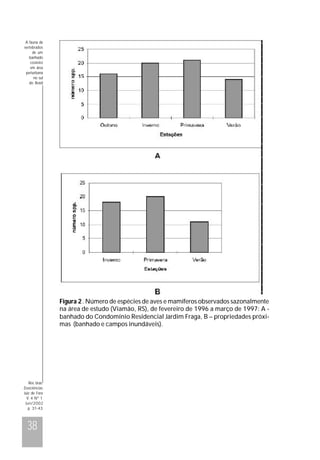
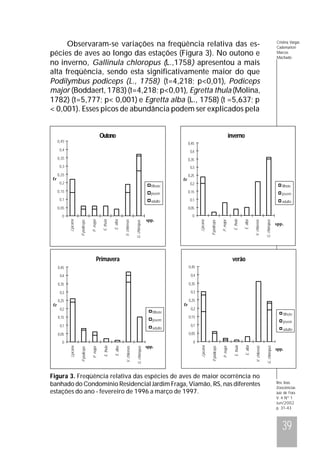
Este documento descreve a fauna de vertebrados de um banhado costeiro em área periurbana no sul do Brasil. Foram observadas 42 espécies de vertebrados, incluindo 34 aves, uma espécie de mamífero, uma de réptil e cinco de peixes. As espécies mais abundantes variaram sazonalmente de acordo com fatores como alimentação, reprodução e deslocamento. A preservação deste banhado é importante para manter a fauna local e migratória.