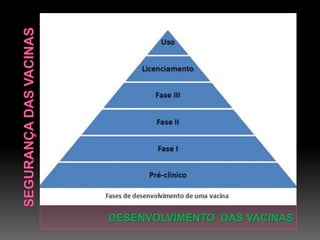
O documento descreve as etapas do desenvolvimento, conservação e boas práticas de vacinas. O desenvolvimento inclui rigorosos testes em animais e humanos em múltiplas fases, avaliação por agências regulatórias e monitoramento pós-registro. A conservação exige uma cadeia de frio eficaz para manter as vacinas entre 2-8°C. As boas práticas envolvem treinamento da equipe, controle de qualidade e segurança do paciente.