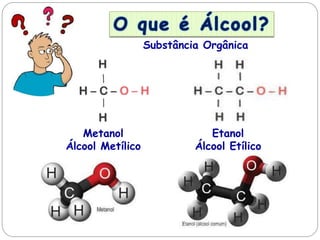
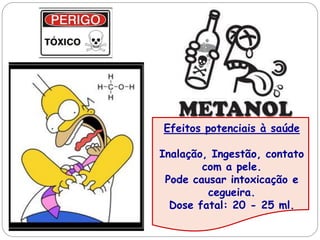
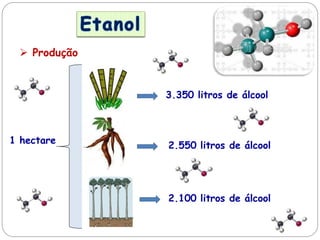
O documento discute a produção e uso do etanol no Brasil. O Brasil é o segundo maior produtor mundial de etanol e usa principalmente cana-de-açúcar como matéria-prima. A gasolina vendida no país contém 25% de etanol. O programa Pró-Álcool incentivou o uso de etanol como combustível nas décadas de 1970 e 1980, mas sua produção caiu depois devido a problemas econômicos e técnicos. Recentemente, o interesse pelo etanol voltou a crescer por preocupações ambientais.