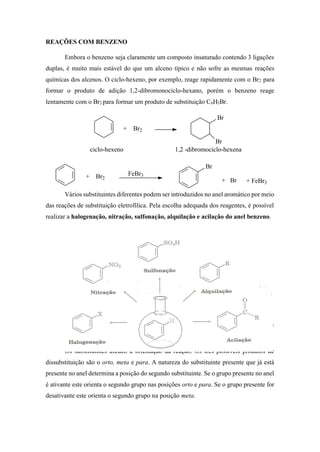
Reações do benzeno e substituição eletrofílica aromática
- 1. REAÇÕES COM BENZENO Embora o benzeno seja claramente um composto insaturado contendo 3 ligações duplas, é muito mais estável do que um alceno típico e não sofre as mesmas reações químicas dos alcenos. O ciclo-hexeno, por exemplo, reage rapidamente com o Br2 para formar o produto de adição 1,2-dibromonociclo-hexano, porém o benzeno reage lentamente com o Br2 para formar um produto de substituição C6H5Br. Vários substituintes diferentes podem ser introduzidos no anel aromático por meio das reações de substituição eletrofílica. Pela escolha adequada dos reagentes, é possível realizar a halogenação, nitração, sulfonação, alquilação e acilação do anel benzeno. Os substituintes presentes afetam a reatividade do anel aromático. Alguns substituintes ativam o anel, tornando-o muito mais reativo que o benzeno, outros o. Os substituintes afetam a orientação da reação. Os três possíveis produtos de dissubstituição são o orto, meta e para. A natureza do substituinte presente que já está presente no anel determina a posição do segundo substituinte. Se o grupo presente no anel é ativante este orienta o segundo grupo nas posições orto e para. Se o grupo presente for desativante este orienta o segundo grupo na posição meta. + Br2 Br Br ciclo-hexeno 1,2 -dibromociclo-hexena + Br2 FeBr3 Br + Br + FeBr3
- 2. Prática No 03 – Preparação de p-nitroclorobenzeno Procedimento experimental 1. Misture com cuidado 12 mL de HNO3 concentrado e 12 mL de H2SO4 concentrado em um balão de boca esmerilhada de 125 mL e esfrie a mistura usando uma cuba cm gelo. 2. Adicione a seguir, gota à gota 4,5 mL (4,8g) de monoclorobenzeno à mistura nitrante, agitando bastante. Caso ocorra aquecimento, coloque o balão em banho de gelo para levar à mistura a temperatura ambiente para só fazer então nova adição de monoclorobenzeno. 3. Ao terminar a adição do monoclorobenzeno, adapte ao balão um condensador de refluxo e deixe sob agitação por 15 minutos ou até que a camada superior de monoclorobenzeno desapareça. 4. Deixe a mistura em repouso, à temperatura ambiente, por 10 minutos para a reação se completar. 5. Derrame-a sobre cerca de 50g de gelo moído em um Becker de 100 mL, agite até que o gelo se desfaça e então filtre os cristais à vácuo e lave-os com pouca água gelada. 6. Recristalize o produto usando uma pequena quantidade de etanol, cerca de 30 mL. 7. Filtre os cristais a vácuo, seque-os bem para depois pesá-los. 8. Calcule os rendimentos teóricos e práticos da reação. Obs: a. Tome cuidado com o manuseio da mistura nitrante (HNO3 + H2SO4). Esta é muito corrosiva. Em caso de acidente lave o local com bastante água corrente. b. Observe com cuidado a temperatura de nitração para evitar a formação de produtos dinitrados como o 2,4-dinitroclorbenzeno. c. O condensador deve conter uma redução de conexão ligada à uma mangueira de látex com saída adaptada a um funil simples invertido e colocado a um Becker contendo água, para a absorção dos gases. Baseado no resultado obtido formule as reações químicas que ocorrem no experimento desenvolvendo os seus mecanismos. Propriedades físicas
- 3. Clorobenzeno P.e. = 132o C; Solubilidade: etanol, benzeno, clorofórmio e éter etílico; D20 = 1,107g/mL P- Nitroclorobenzeno P.e. = 82 - 84o C; Solubilidade: etanol à quente, éter etílico e dissulfeto de carbono. Cl Cl O2N