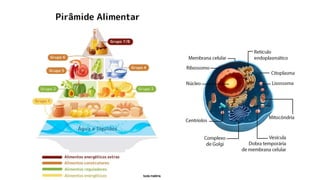
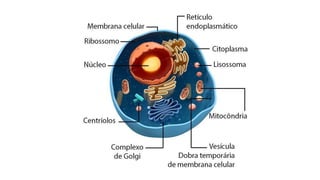
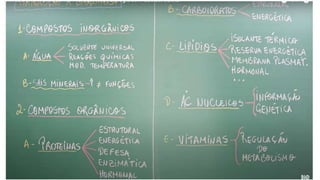
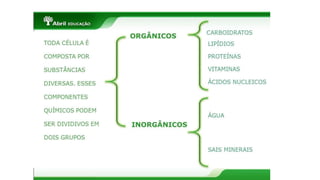
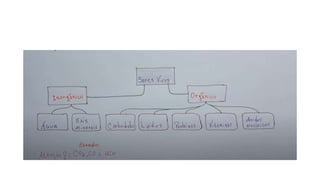
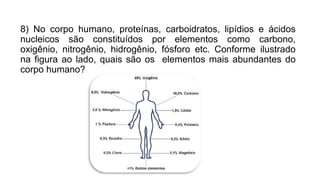
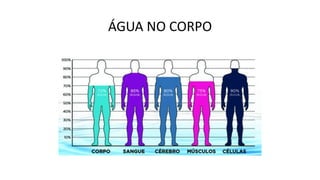
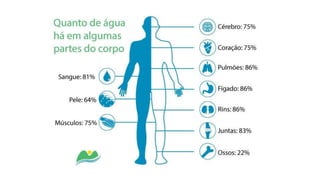
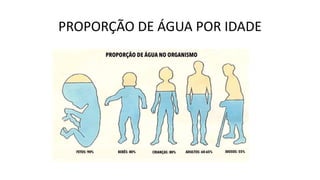
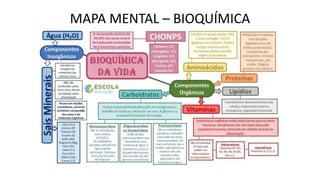
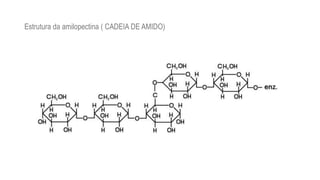
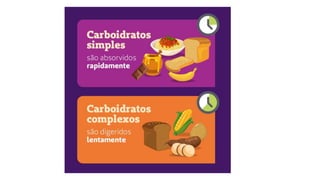
A bioquímica estuda as reações químicas nos seres vivos e os compostos envolvidos, sendo essencial para entender os processos vitais. As biomoléculas, como proteínas, lipídios, carboidratos e ácidos nucleicos, são fundamentais para a estrutura e função celular, enquanto a água desempenha papéis críticos no organismo, como solvente e regulador térmico. O documento também aborda a interação de elementos químicos e a importância de substâncias inorgânicas e orgânicas na biologia.



























































![Bioquímica [Salvo automaticamente] [Salvo automaticamente].pptx](https://image.slidesharecdn.com/bioqumicasalvoautomaticamentesalvoautomaticamente-240606183222-42efc04e/85/Bioquimica-Salvo-automaticamente-Salvo-automaticamente-pptx-103-320.jpg)