Incorporar apresentação
Baixado 10 vezes





![LEI DA VELOCIDADE a A + b B c C + d D V = K [A] n . [B] m Onde: n = ordem da reação em relação a A m= ordem da reação em relação a B OBS: em reações elementares n = a e m = b V = K [A] a . [B] b CINÉTICA QUÍMICA](https://image.slidesharecdn.com/26-090625132316-phpapp01/85/26-7-320.jpg)

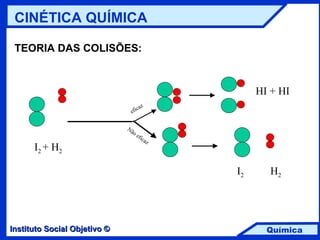
A cinética química estuda a velocidade das reações e os fatores que a influenciam, como temperatura, pressão e área de contato. A lei da velocidade é expressa como v = k [a]^n [b]^m, onde n e m são as ordens da reação em relação aos reagentes. A energia de ativação e o papel dos catalisadores também são fundamentais na cinética química.






![LEI DA VELOCIDADE a A + b B c C + d D V = K [A] n . [B] m Onde: n = ordem da reação em relação a A m= ordem da reação em relação a B OBS: em reações elementares n = a e m = b V = K [A] a . [B] b CINÉTICA QUÍMICA](https://image.slidesharecdn.com/26-090625132316-phpapp01/85/26-7-320.jpg)