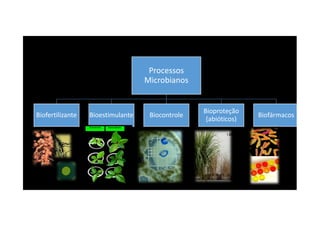
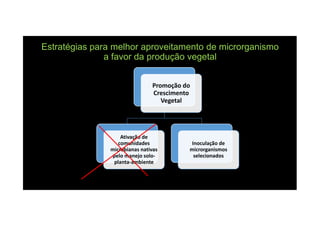
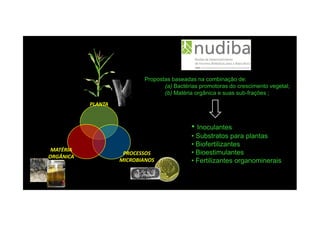
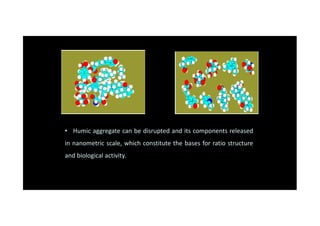
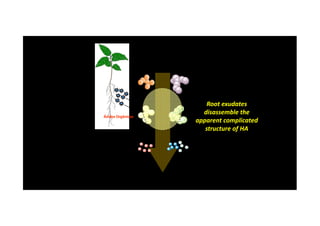
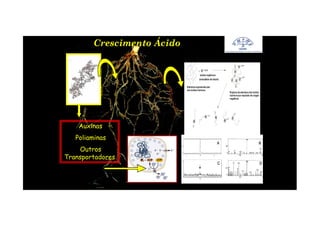
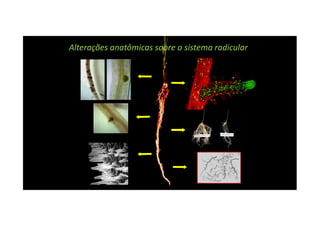
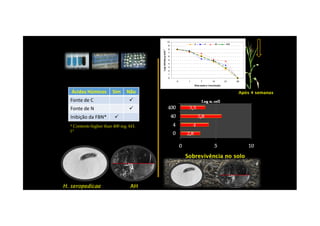
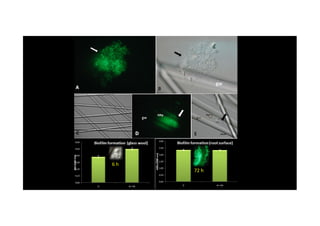
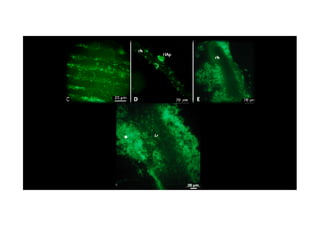
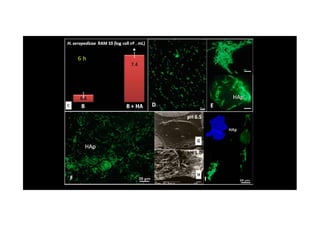
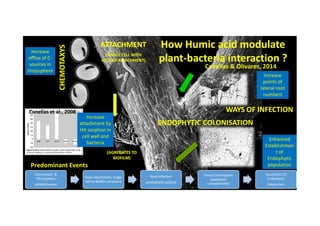
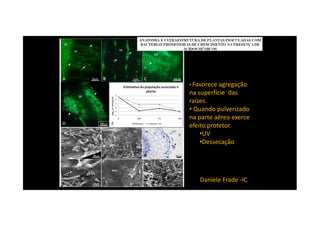
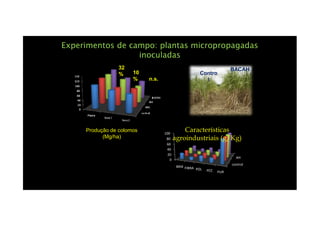
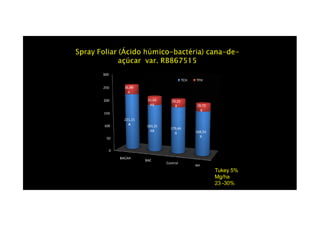
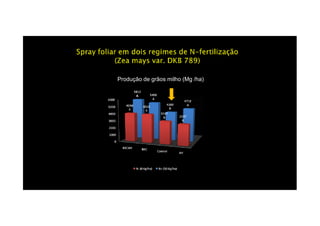
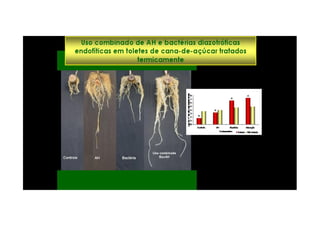
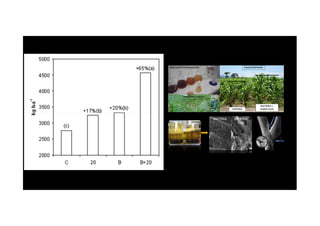
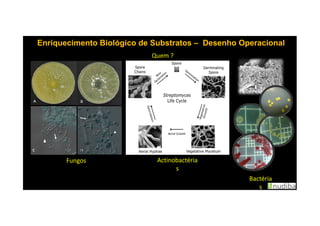
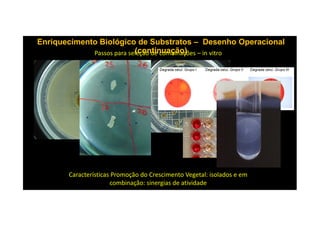
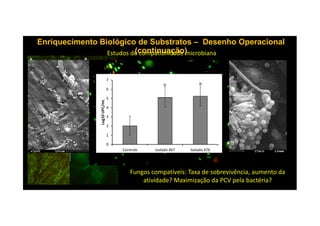
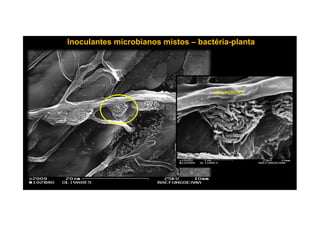
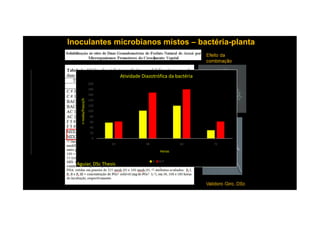
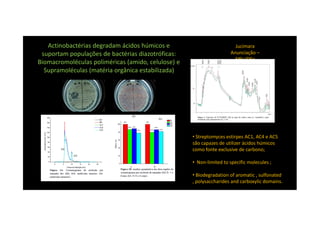
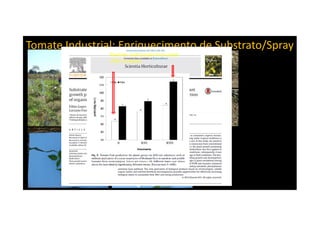
O documento discute o potencial dos processos microbianos como insumos biológicos para uma agricultura sustentável. Apresenta estratégias para melhor aproveitar microrganismos a favor do crescimento vegetal, como a inoculação de bactérias promotoras ou a ativação de comunidades nativas pelo manejo do solo e da planta. Também descreve estudos sobre biofertilizantes produzidos a partir da combinação de ácidos húmicos e bactérias diazotróficas, que promovem alterações morfológicas