O documento descreve a composição e estrutura da atmosfera terrestre. Resumidamente:
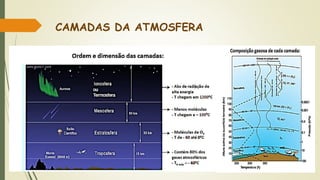
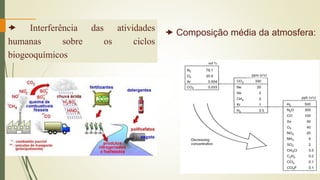
1) A atmosfera é composta principalmente por nitrogênio e oxigênio, com pequenas quantidades de outros gases como argônio e dióxido de carbono.
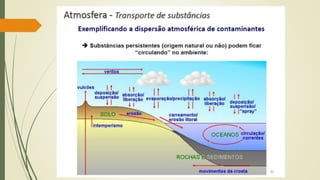
2) A atmosfera é dividida em camadas - a troposfera, estratosfera, mesosfera e termosfera - que variam em temperatura e composição de gases conforme a altitude.
3) A atmosfera é vital para a vida na Terra pois protege







































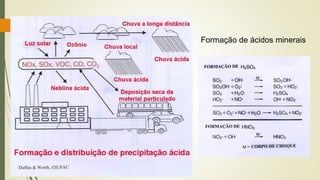
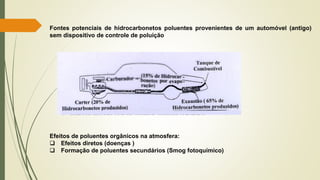
![ Combustão:
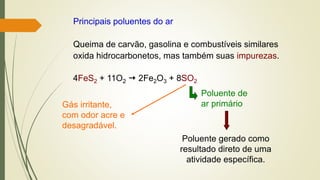
Combustível + ar gases + partículas
[O2 e N2] [ex.: NO + SO2 + CO2]
Conhecer a composição química do material combustível
conhecer os gases emitidos.
C, H e O CO2 e H2O
C, H, O e S SO2
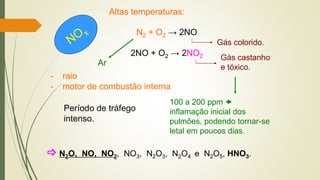
Obs.: Exceção: NO é formado em todas as combustões,
independente da composição do material queimado.
N2 + O2 2NO
oxida facilmente, formando NO2.](https://image.slidesharecdn.com/qumicadaatmosfera-230223235603-30aae19f/85/Quimica-da-Atmosfera-pdf-53-320.jpg)