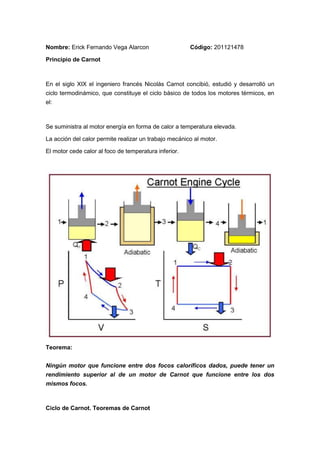
Ciclo de Carnot
- 1. Nombre: Erick Fernando Vega Alarcon Código: 201121478 Principio de Carnot En el siglo XIX el ingeniero francés Nicolás Carnot concibió, estudió y desarrolló un ciclo termodinámico, que constituye el ciclo básico de todos los motores térmicos, en el: Se suministra al motor energía en forma de calor a temperatura elevada. La acción del calor permite realizar un trabajo mecánico al motor. El motor cede calor al foco de temperatura inferior. Teorema: Ningún motor que funcione entre dos focos caloríficos dados, puede tener un rendimiento superior al de un motor de Carnot que funcione entre los dos mismos focos. Ciclo de Carnot. Teoremas de Carnot
- 2. Para poder llegar a una formulación matemática del segundo principio de la termodinámica empleamos lo que se conoce como un ciclo de Carnot: una máquina que funciona cíclicamente entre dos focos mediante procesos reversibles, por tanto puede ser motor o frigorífico. Un ciclo de Carnot está constituido por dos transformaciones isotermas reversibles y dos transformaciones adiabáticas reversibles. Durante las transformaciones isotermas el sistema absorbe y cede calor a temperatura constante y en las transformaciones adiabáticas el sistema intercambia trabajo. Primer teorema de Carnot: El rendimiento de una máquina de Carnot que funcione entre dos focos térmicos es superior al de cualquier máquina real funcionando entre los mismos puntos. La forma de demostrar este teorema es poniendo dos máquinas a trabajar entre los mismos focos, siendo una real y otra una máquina de Carnot. Si las acoplamos de alguna manera y aplicamos el primer principio vemos que la única forma de que no se viole ninguno de los enunciados del segundo principio implica que el rendimiento de la máquina de Carnot es superior al de la máquina real. Segundo teorema de Carnot Cualquier máquina reversible que funcione entre los mismos focos tiene el mismo rendimiento sea cual sea la sustancia con la que trabaja. La demostración de este teorema es que si tuviesen un rendimiento diferente, al invertir una de las máquinas se podría acoplar con la otra dando lugar a la violación de alguno de los enunciados del segundo principio. - Una máquina térmica totalmente reversible está libre de efectos disipativos y desequilibrio durante su operación, tales efectos deben ser nulos en la máquina y en la transferencia de calor que se realiza con una fuente térmica y un sumidero de calor, es decir, la transferencia de calor debe ser reversible. Pero si dentro de la máquina térmica existe alguna irreversibilidad o hay interacciones de la máquina térmica con su ambiente, la máquina se clasifica como irreversible. El ciclo de Carnot es el ciclo más eficiente. - El ciclo de Carnot es un ciclo teórico y reversible, su limitación es la capacidad que posee un sistema para convertir en calor el trabajo, se utiliza en las máquinas que usan vapor o una mezcla de combustible con aire u oxígeno. NOTA: “Las cosas ideales sólo nos ayudan a entender las reales”.Se dice que un proceso termodinámico es reversible, cuando acometiendo pequeños cambios en el ambiente podemos conseguir que recorra su trayectoria inversa. En la práctica es imposible, en la naturaleza todos los procesos que ocurren son irreversibles. Sin
- 3. embargo el estudio de estos procesos es muy útil pues nos da el valor del rendimiento máximo que se puede obtener de una máquina. Los procesos reales tienen alguna irreversibilidad, ya sea mecánica por rozamiento, térmica o de otro tipo. Sin embargo, las irreversibilidades se pueden reducir, pudiéndose considerar reversible un proceso cuasi estático y sin efectos disipativos. Los efectos disipativos se reducen minimizando el rozamiento entre las distintas partes del sistema y los gradientes de temperatura; el proceso es cuasi estático si la desviación del equilibrio termodinámico es a lo sumo infinitesimal, esto es, si el tiempo característico del proceso es mucho mayor que el tiempo de relajación (el tiempo que transcurre entre que se altera el equilibrio hasta que se recupera). Por ejemplo, si la velocidad con la que se desplaza un émbolo es pequeña comparada con la del sonido del gas, se puede considerar que las propiedades son uniformes espacialmente, ya que el tiempo de relajación mecánico es del orden de V1/3 /a (donde V es el volumen del cilindro y a la velocidad del sonido), tiempo de propagación de las ondas de presión, mucho más pequeño que el tiempo característico del proceso, V1/3 /w (donde w es la velocidad del émbolo), y se pueden despreciar las irreversibilidades. Si se hace que los procesos adiabáticos del ciclo sean lentos para minimizar las irreversibilidades se hace imposible frenar la transferencia de calor. Como las paredes reales del sistema no pueden ser completamente adiabáticas, el aislamiento térmico es imposible, sobre todo si el tiempo característico del proceso es largo. Además, en los procesos isotermos del ciclo existen irreversibilidades inherentes a la transferencia de calor. Por lo tanto, es imposible conseguir un ciclo real libre de irreversibilidades, y por el primer teorema de Carnot la eficiencia será menor que un ciclo ideal.
- 4. El ciclo de Carnot es un ciclo termodinámico reversible que usa un gas perfecto y que consta de cuatro etapas: 1. Expansión isoterma. En la situación inicial el gas se encuentra a la máxima presión, mínimo volumen y la máxima temperatura dada por el foco caliente. En contacto con el foco, el gas se expande (disminuyendo la presión y aumentando el volumen) de forma isoterma (temperatura constante) por lo que se absorbe calor de la fuente. 2. Expansión adiabática. Se aísla térmicamente el recipiente que contiene el gas (por ello no existe transferencia de calor con el exterior) así que continúa expandiéndose pero en esta etapa se consigue además que el gas disminuya su temperatura. 3. Compresión isoterma. En esta etapa se comprime el gas (aumentando presión y disminuyendo el volumen que éste ocupa) manteniendo constante la temperatura. Dada esta situación el gas cede calor al foco frío. Compresión adiabática. Aislado térmicamente, el sistema evoluciona comprimiéndose y aumentando su temperatura hasta el estado inicial. La representación gráfica del ciclo de Carnot en un diagrama p-V es el siguiente Tramo A-B isoterma a la temperatura T1 Tramo B-C adiabática Tramo C-D isoterma a la temperatura T2 Tramo D-A adiabática Motor y frigorífico Un motor de Carnot es un dispositivo ideal que describe un ciclo de Carnot. Trabaja entre dos focos, tomando calor Q1del foco caliente a la temperatura T1, produciendo un trabajo W, y cediendo un calor Q2 al foco frío a la temperaturaT2. En un motor real, el foco caliente está representado por la caldera de vapor que suministra el calor, el sistema cilindro-émbolo produce el trabajo y se cede calor al foco frío que es la atmósfera.
- 5. La máquina de Carnot también puede funcionar en sentido inverso, denominándose entonces frigorífico. Se extraería calor Q2 del foco frío aplicando un trabajo W, y cedería Q1 al foco caliente. En un frigorífico real, el motor conectado a la red eléctrica produce un trabajo que se emplea en extraer un calor del foco frío (la cavidad del frigorífico) y se cede calor al foco caliente, que es la atmósfera. Efecto Joule: Se conoce como Efecto Joule al fenómeno por el cual si en un conductor circula corriente eléctrica, parte de la energía cinética de los electrones se transforma en calor debido a los choques que sufren con los átomos del material conductor por el que circulan, elevando la temperatura del mismo. En pocas palabras el efecto joule es el calentamiento que tiene un conductor al paso una corriente, en términos de distribución son las pérdidas de energía al calentamiento de un conductor ya que la conducción de energía por un conductor de calibre inferior representa un calentamiento actuando como una resistencia al paso de la corriente. Formulación Efecto Joule: Este efecto es utilizado para calcular la energía disipada en un conductor atravesado por una corriente eléctrica de la siguiente manera: La potencia P disipada en un conductor es igual a la diferencia de potencial V a la que está sometido multiplicada por la intensidad de corriente I que lo atraviesa. La energía desarrollada E es el producto de la potencia P por el tiempo t transcurrido, luego la energía E es el producto de la tensión V por la intensidad I y por el tiempo t.
- 6. CONCLUSIONES: ¿Por qué calentar algo con efecto Joule con energía eléctrica pudiéndolo hacer con gas es energéticamente absurdo? Es un derroche de recursos calentar con energía eléctrica, si se puede hacer con gas, dado que por efecto Joule la energía se disipa y se pierde por entre las paredes del conducto, llámese cable, alambre, etc. Mientras que el gas puede llegar hasta donde lo necesito y liberar su energía donde quiero sin perder energía por las paredes. ¿Por qué se dice que la naturaleza trabaja siguiendo principio de Carnot? En la naturaleza: a) No quedan en absoluto satisfechas las condiciones de equilibrio mecánico, químico o térmico, es decir, de equilibrio termodinámico. b) Se producen siempre efectos de disipación energética, viscosidad, resistencia eléctrica, etc... Nota: Solamente si un proceso se realiza cuasi-estáticamente pasaría por una serie de estados de equilibrio termodinámico de modo que el trabajo que realiza puede recibirlo en el proceso inverso. - La transferencia de calor Isotérmica reversible es muy difícil, así que no es practico construir una máquina que opere en un ciclo que se aproxime en gran medida al ciclo de Carnot, en términos de tiempo y recursos.
