Estereoquímica - Enantiômeros e Quiralidade
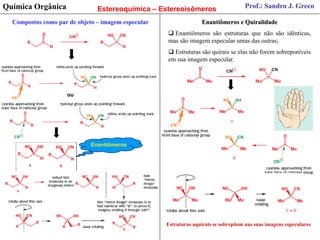
- 1. Prof.: Sandro J. Greco Química Orgânica Estereoquímica – Estereoisômeros Compostos como par de objeto – imagem especular Enantiômeros e Quiralidade Enantiômeros são estruturas que não são idênticas, mas são imagem especular umas das outras; Estruturas são quirais se elas não forem sobreponíveis em sua imagem especular. ou Enantiômeros Estruturas aquirais se sobrepõem nas suas imagens especulares
- 2. Prof.: Sandro J. Greco Química Orgânica Estereoquímica – Estereoisômeros Centro estereogênico Plano de simetria Não possui centro estereogênico Moléculas quirais não possuem plano de simetria • Se uma molécula contém um átomo de carbono com quatro grupos diferentes, essa molécula não possui nenhum plano de simetria e deve portanto ser quiral. Um átomo de carbono Objetos quirais contendo quatro grupos diferentes é portanto estereogênico ou centro quiral.
- 3. Prof.: Sandro J. Greco Química Orgânica Estereoquímica – Estereoisômeros Configuração x Conformação ISÔMEROS Estereoisômeros Isômeros estruturais ou Isômeros espaciais Isômeros Isômeros configuracionais conformacionais Moléculas iguais H H F Não são separáveis H H H H (em equilíbrio) F Conformação Isômeros geométricos Isômeros ópticos F H Moléculas diferentes e H H H H São separáveis H F enantiômeros Diastereoisômeros Configuração •A configuração de uma molécula só é alterada se ligações forem quebradas e formadas; • Configurações diferentes, necessariamente, são moléculas diferentes.
- 4. Prof.: Sandro J. Greco Química Orgânica Estereoquímica – Estereoisômeros Mentalmente, mova do substituinte de prioridade até o de Nomenclatura R e S para descrever a configuração prioridade 3. Se o movimento for no sentido horário a horá absoluta de um centro quiral configuração absoluta da molécula é R. Caso o movimento se processe no sentido anti-horário a configuração absoluta é S . anti- horá Nomenclatura atual, baseada no sistema Cahn, Ingold e Prelog. Este sistema faz parte das regras da IUPAC. Atividade óptica – rotação da luz plano polarizada Propriedades Físicas (R)-2-Butanol (S)-2-Butanol Regras de prioridade 99.5 °C 99.5 °C Ponto de ebulição (1 atm) 1 Densidade (g mL–1 a 20 °C) 0.808 0.808 Índice de refração (20 °C) 1.397 1.397 Assinale o número de prioridade de cada substituinte do centro quiral. Átomos com maiores números atômicos possuem as maiores prioridades; 2 O átomo de menor prioridade deve estar o mais afastado possível do observador; 3 2
- 5. Prof.: Sandro J. Greco Química Orgânica Estereoquímica – Estereoisômeros Rotação específica Mistura racêmica Rotação específica [α]: é a medida quantitativa da atividade óptica por polarimetria. É característica de cada molécula opticamente ativa. Me H ATENÇÃO ! A OH H HO nomenclatura R, S Ph não diz se o isômero R isômero R Pureza Óptica e Excesso Enantiomérico isômero é (+) ou (-) 25 25 [α] D (puro) + 42o [α] D (puro) - 48o Pureza óptica = rotação específica observada α rotação observada (graus) rotação específica do enantiômero puro comprimento do tubo (dm) [α] = α l [α] = α t t c concentração (g / 100 mL) λ λ l. c l. d d densidade (g / mL) para soluções temperatura ( oC) para líquidos t puros λ comprimento de onda da luz incidente (nm) Composto [a]D (Graus) Cânfora +44.26 - λ da luz (raia D do sódio: mais usada) Morfina –132 determinar [ α] em - natureza do solvente Penicilina V +223 Fatores que diferentes solventes influenciam Colesterol –31.5 usar, sempre que possível, o valor de - concentração amostras concentradas [α] c 5 % Excesso Enantiomérico = (M+) – (M-) - temperatura (M+) + (M-)
- 6. Prof.: Sandro J. Greco Química Orgânica Estereoquímica – Estereoisômeros Diastereoisômeros – aquirais Diastereoisômeros – quirais
- 7. Prof.: Sandro J. Greco Química Orgânica Estereoquímica – Estereoisômeros Diastereoisômeros e propriedades físicas Epímeros Moléculas aquirais com centros estereogênicos Compostos que contem centros estereogênicos e são muitas vezes quirais são chamados de compostos meso. Esses compostos necessariamente possuem um plano de simetria.
- 8. Prof.: Sandro J. Greco Química Orgânica Estereoquímica – Estereoisômeros Compostos quirais sem centros estereogênicos Estereoisomerismo e propriedades físicas Diastereoisômeros – propriedades físicas diferentes Exemplos: O O Cl H o o H Cl p.e. = 4 C p.e. = 1 C μ = 3,07 D μ = 1,08 D (mais polar) (menos polar) HO HO OH O O HO HO HO HO HO OH OH (D-glicose) (D-manose) 25 25 [α]D + 52 (c 1, H2O) [α]D + 14,8 (c 4, H2O) OTs OTs EtONa EtONa H (E2) (E2) H cis rápido lento trans H e OTs: antiperiplanares OH CO2Me O O Eluente: 0,5% MeOH/ CHCl3 ( + )-anti _ Revelador: luz U.V. OH CO2Me O syn anti O ( + )-syn _
- 9. Prof.: Sandro J. Greco Química Orgânica Estereoquímica – Estereoisômeros Estereoisomerismo e propriedades físicas Enantioômeros – propriedades físicas iguais O O EXCEÇÃO CO2CH3 CO2CH3 Et Et SINAL DO [α]D 25 25 [α]D +82 (c 5,7, EtOH) [α]D -82 (c 5,7, EtOH) Separação de enantiômeros
- 10. Prof.: Sandro J. Greco Química Orgânica Estereoquímica – Estereoisômeros Solubilidade Separação de enantiômeros Cromatografia
- 11. Prof.: Sandro J. Greco Química Orgânica Estereoquímica – Estereoisômeros Importância do estereoisomerismo Enantiômeros x Receptores Biológicos Propriedades biológicas de muitas substâncias são muito dependentes das suas configurações absolutas. Indústrias: farmacêutica, defensivos agrícolas, flavours, etc. TRAGÉDIA DA TALIDOMIDA O O O N O N N N OO H OO H (-)-talidomida (+)-talidomida (teratogênico) (sedativo) O O O O O HO H HO H O N O O HO O ON H O O H3CO OCH3 N3 OCH3 β-vetivona Vepesid VP-16 AZT (antitumoral) (anti-HIV)
