Traduccion proteinas
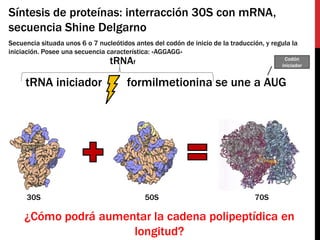
- 1. Síntesis de proteínas: interracción 30S con mRNA, secuencia Shine Delgarno Secuencia situada unos 6 o 7 nucleótidos antes del codón de inicio de la traducción, y regula la iniciación. Posee una secuencia característica: «AGGAGG» tRNAf Codón iniciador tRNA iniciador formilmetionina se une a AUG 30S 50S 70S ¿Cómo podrá aumentar la cadena polipeptídica en longitud?
- 2. tRNAf se une a lugar P del ribosoma AUG ACA GGG AAA UCG GUC Sitio E tRNAf Sitio P AUG ACA GGG AAA UCG GUC mRNA Sitio A Túnel
- 3. Un aminoacil-tRNA con un anticodón complementario AUG ACA GGG AAA UCG GUC AUG ACA GGG AAA Aminoacil-tRNA
- 4. La molécula de formilmetionina unida al tRNA iniciador va a ser transferida al grupo amino del aminoácido que ocupa el lugar A AUG ACA GGG AAA UCG GUC
- 5. La molécula de formilmetionina unida al tRNA iniciador va a ser transferida al grupo amino del aminoácido que ocupa el lugar A AUG ACA GGG AAA UCG GUC
- 6. La molécula de formilmetionina unida al tRNA iniciador va a ser transferida al grupo amino del aminoácido que ocupa el lugar A AUG ACA GGG AAA UCG GUC La formación del enlace peptídico es termodinámicamente espontánea *Catalizada por el lugar rRNA 23S (centro peptidiltransfersa)
- 7. • Grupo amino del aminoacil-tRNA de lugar A está bien posicionado para atacar enlace éster entre el tRNA iniciador y molécula de formilmetionina. • El centro peptidiltransferasa posee bases que promueven reacción ayudando a formar un grupo -NH₂ en el aminoacil-tRNA del lugar A y ayudando a estabilizar intermediario tetraédrico que se forma.
- 8. Con formación de enlace peptídico, cadena peptídica está unida a tRNA en lugar A de la subunidad 30S. AUG ACA GGG AAA UCG GUC El tRNA en el lugar P de la subunidad 30S está ahora descargado. Para continuar traducción, el mRNA debe ser translocado de forma de que el codón para el siguiente aminoácido esté en el sitio A.
- 9. Esta translocación tiene lugar a través de enzima factor de elongación G (FEG), guiada por la hidrólisis de GTP. GTP GDP+ Pi FEG AUG ACA GGG AAA UCG GUC AUG ACA GGG AAA UCG Completando este paso, el peptidil–tRNA está plenamente en el sitio P, y el tRNA iniciador en el sitio E, separado del mRNA.
- 10. Al disociarse del tRNA iniciador, ribosoma ha vuelto a su estado inicial excepto que cadena peptídica está unida a un tRNA diferente. AUG ACA GGG AAA UCG GUC AUG ACA GGG AAA UCG GUC Cadena peptídica permanece en el lugar P en la subunidad 50S durante todo este ciclo, a la entrada del túnel de salida, alargándose. Este ciclo se repite cuando un nuevo aminoacil-tRNA se coloca en el lugar A, permitiendo que el polipéptido se alargue indefinidamente* *Hasta la entrada de un codón stop en el sitio A(UAA, UAG, UGA) ya que no hay ningún anticodón complementario a los codones de stop.
- 11. La interacción de apareamiento de bases del anticodón del tRNA entrante con el codón del mRNA en el sitio A determina qué aminoácido va añadirse a la cadena polipeptídica. ¿Juega algún papel en este proceso el aminoácido unido al tRNA? 1. Cys se unió a su tRNA correspondiente Cys 2. Cys unido se convertía en Ala mediante reacción del Cys-tRNA con níquel Raney, lo que eliminaba S del residuo de Cys activada sin afectar su unión con tRNA, produciéndose un aminoacil-tRNA erróneamente cargado en que Ala estaba unida covalentemente al tRNA específico para Cys.
- 12. ¿Qué reconoce este tRNA erróneamente cargado: codón de Ala o Cys? tRNA híbrido a sistema de síntesis proteíca libre de c. El molde fue copolímero al azar de U y G en proporción de 5:1, que conduce normalmente a incorporación de Cys (cod UGU) pero no de Ala (cod GCN). Cuando se añadió Ala-tRNA a la mezcla de incubación, se Cys incorporó Ala al polipéptido ya que estaba unida al tRNA específico para la cisteína. Por lo que se demostró que: El aminoácido del aminoacil - tRNA no interviene a la hora de seleccionar el codón.
- 13. ¿Cuáles son las reglas que gobiernan el reconocimiento de un codón por el anticodón de un tRNA? 1. Cada una de las bases del codón formase una pareja de bases con una base complementaria del anticodón, por lo que estarían alineados en forma antiparalela. -Según este modelo, un anticodón particular sólo podría reconocer un determinado codón. 2. Algunas moléculas puras de tRNA pueden reconocer a más de un codón. Por ejemplo, el tRNA para la Ala de levadura puede unirse a 3 codones: GCU, GCC, GCA. ¿Podría ocurrir que reconocimiento de 3° base sea menos restrictivo?
- 14. Francis Crick: Criterios de apareamiento Se construyeron modelos de varias parejas de bases para determinar cuáles son similares en cuanto a distancia y ángulo entre enlaces glucosídicos, y la inosina fue incluida ya que aparece en varios anticodones. Primera base Tercera base del anticodón del codón Se admite cierta libertad estérica (wobble) C G en emparejamiento de 3° base. A U U AoG G UoC I U, C, o A
- 15. 1. Las dos primeras bases del codón se aparean en la forma estándar. El reconocimiento es exacto, por lo que los codones que difieren en alguna de sus dos primeras bases deben ser reconocidos por diferentes tRNAs. Tanto UUA como CUA, codifican a la leucina, pero son leídos por diferentes tRNAs. 2. La primera base de un anticodón determina que una molécula concreta de tRNA pueda leer 1, 2 o 3 tipos de codones.
- 16. o Parte de la generación del código genético surge de imprecisión en apareamiento de 3° base de codón con la 1° base del anticodón. o La inosina eleva al máximo # de codones que pueden ser leídos por una molécula de tRNA determinada. o La inosina se forma por desaminación de adenosina al concluir el transcrito primario.
- 17. ¿ Por qué el balanceo es tolerante con 3° pero no en las otras 2? La subunidad 30 S contiene 3 bases universalmente conservadas (adeninas A1492 y A1493 y la guanina 530) del RNA 16S que forman puentes de H con cara del surco < del dúplex codón-anticodón. No existe dispositivo de inspección para la 3° posición. El ribosoma ejerce un papel activo en la descodificación del las interacciones codón- anticodón.
Notas do Editor
- The correct amino acid is added to its tRNA by a specific enzyme called an aminoacyl-tRNAsynthetase. The process is called aminoacylation, or charging. Since there are 20 amino acids, there are 20 aminoacyl-tRNAsynthetases. All tRNAs with the same amino acid are charged by the same enzyme, even though the tRNA sequences, including anticodons, differ.
- The activated intermediates in protein synthesis are amino acid esters, in which the carboxyl group of an amino acid is linked to either the 2′- or the 3′-hydroxyl group of the ribose unit at the 3′ end of tRNA. An amino acid ester of tRNA is called an aminoacyl-tRNA or sometimes a charged tRNA (Figure 29.7).
