Tecniche e microscopi
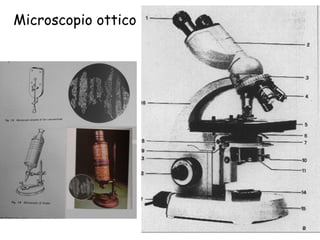
- 2. Microscopio binoculare Stativo Oculari obiettivi Condensatore Apparato di illuminazione Vite macrometrica Vite micrometrica Tavolino traslatore Viti coassiali del tavolino traslatore Porta- preparati Vite regola-altezza del condensatore Interrutore – regolatore intensità luminosa
- 3. C Aberrazione cromatica . F 1 C Aberrazione sferica . F 1 . F 1 . F 1 . F 1 . F 1 . F 1 . F 1
- 4. Tipi di obiettivi: Acromatici – corretti per l’aberrazione cromatica e sferica nel campo delle lunghezze d’onda entro il giallo e verde. Semiapocromatici - corretti per l’aberrazione cromatica e sferica nel campo delle lunghezze d’onda entro il il blu e il rosso. Apocromatici - corretti per l’aberrazione cromatica e sferica in tutto lo spettro del visibile. Planapocromatici – apocromatici corretti per la curvatura di campo. Tipi di oculari: Comuni o Huyghens – abbinati solo ad oculari acromatici < 40x Compensatori – hanno aberrazioni di segno opposte a quelli degli obiettivi. Planari – per obiettivi planari.
- 5. Il biologo ha sempre avuto la necessità di osservare al microscopio oggetti viventi, cellule o tessuti, ma questi, essendo molto sottili e tra- sparenti, non sono general- mente visibili. Nonostante ciò, la luce che emerge dal preparato con- tiene anche la loro immagi- ne, pur se nascosta.
- 6. Microscopio a contrasto di fase Con la microscopia ottica tradizionale i preparati citologici o istologici si possono osservare solo se opportunamente colorati. Essi modificano sia l’ampiezza (la luminosità) sia la lunghezza d’onda (il colore) del raggio di luce che li attraversa . I preparati non colorati provocano solo una leggera sfasatura (differenza di fase) della lunghezza d’onda del raggio che li attraversa; il microscopio a contrasto di fase converte la differenza di fase (invisibile all’occhio) in differenza di ampiezza (visibile all’occhio) del raggio che li attraversa B Percorso della luce quando attraversa un preparato colorato (A) e non colorato (B). In (A) il raggio (rosso) che emerge è modificato sia in ampiezza sia in lunghezza d’onda. In (B) il raggio che emerge (azzurro) è solo sfasato. La linea tratteggiata in (A) e in (B) rappresenta il percorso del raggio in assenza di modificazioni A
- 7. PREMESSA: Diffrazione : deviazione dal percorso ottico che subisce un raggio luminoso quando attraversa oggetti , fessure o fori le cui dimensioni sono circa quelle della lunghezza d’onda incidente. In un normale microscopio ottico quando un raggio luminoso colpisce un oggetto ( raggio incidente ) , all’uscita saranno presenti due raggi : uno diretto (che è sullo stesso percorso dell’incidente) , l’altro diffratto (che è leggermente deviato rispetto al diretto). Il raggio diffratto , oltre ad essere un po’ deviato è anche sfasato rispetto al diretto di un valore che va da 0 a ¼ λ e il valore di tale sfasatura dipende dalla densità dell’oggetto attraversato.
- 10. Raggio diretto e diffratto : Il diffratto è sfasato rispetto al trasmesso di un valore 1/x che è < di ¼ λ Anello di fase (Inserito nell’obiettivo) Dispositivo di illuminazione Il raggio diffratto è sfasato di 1/x + ¼ λ I due raggi interferiscono dando un raggio di maggior ampiezza Lente intermedia
- 11. Microscopio a contrasto di fase Serve ad osservare cellule e tessuti in vivo . Fu messo a punto dall’olandese Fritz Zernike (premio Nobel per fisica) nel 1934. L’anello di fase proietta un cono di luce, cavo al centro, sul preparato. I raggi che colpiscono gli organelli citoplasmatici producono due raggi: uno diretto (che non subisce alterazioni); l’altro che risulterà deviato e sfasato di valore pari a una frazione di x · . Quest’ultimo subisce un ulteriore ritardo di fase, pari a ¼ (ritardo finale= 1/4 +x · ) quando attraversa la parte più spessa dell’anello di fase. I raggi deviati interferiscono con quelli diretti dando origine a raggi finali che avranno una minore ampiezza (minore luminosità). Gli organelli, pertanto, risulteranno visibili, con diverse tonalità di grigio fino al nero.
- 12. Microscopio polarizzatore Sorgente luminosa 1°Filtro Nicols Piano di vibrazione della luce polarizzata 2°Filtro Nicols Piano di vibrazione della luce polarizzata Piano di vibrazione della luce polarizzata Dà informazioni sulla struttura dei campioni, indicando se modificano ( anisotropi ) o meno ( isotropi )il piano di vibrazione della luce polarizzata. Le particelle di luce della lampada vibrano in tutti i piani. Nel passare attraverso il primo filtro di Nicols, la luce viene modificata (p olarizzata ) in quanto le sue particelle vibrano in un solo piano. Passando attraverso il secondo filtro di Nicols, la luce riesce ad emergere solo se i piani del reticolo cristallino del polarizzazione del primo e secondo filtro sono paralleli ( A ); se sono perpendicolari (polarizzatori incrociati) i raggi luminosi vengono bloccati; pertanto si ha il buio ( B );. A B buio
- 13. Microscopio polarizzatore Sorgente luminosa 1°Filtro Nicols Piano di vibrazione della luce polarizzata Campione isotropo Campione anisotropo 2°Filtro Nicols Piano di vibrazione della luce polarizzata Piano di vibrazione della luce polarizzata Nel microscopio polarizzatore i filtri e/o il campione possono ruotare. A filtri incrociati, se il campione in esame è isotropo, risulterà buio. Infatti, in qualsiasi direzione esso viene osservato altera il piano della luce polarizzata, la quale che sarà bloccata dal secondo filtro Nicols ( A ). A filtri paralleli il campione isotropo risulterà illuminato. A filtri incrociati se l’oggetto in esame è anisotropo (ad esempio le fibre collagene, alcuni parti della fibra muscolare striata), osservato in una data direzione altera il piano di vibrazione della luce polarizzata. Le particelle di luce che emergono dal campione ruotano il loro piano di vibrazione risultando parallelo al reticolo del secondo filtro di Nicols, da cui emergono; il campione o sue parti risultano pertanto illuminate ( B ). A B buio
- 14. Alcuni materiali biologici, soprattutto vegetali, co- me la cellulosa, colpiti da radiazione U.V. emettono naturalmente fluorescen- za: si parla in tal caso di fluorescenza primaria o autofluorescenza . La maggior parte dei campioni biologici però emette fluorescen- za solo dopo marcatura con fluo rocromi: in tal caso si parla di fluorescenza secondaria o indotta . Sezione di fascio vascolare di Dicotiledone
- 16. Microscopio a fluorescenza (epifluorescenza) Anticorpi fluriscinati anti-actina NOR-FISH TELO--FISH Occhio Obiettivo Lampada UV
- 17. Microscopio a fluorescenza 1) La lampada a vapori di mercurio emette radiazioni ad elevata energia; 2) il filtro di eccitazione lascia passare le radiazioni ad una ristretta lunghezza (ad esempio in verde) d’onda; 3) tali radiazioni penetrano nell’obiettivo, sono riflesse dallo specchio dicroico e eccitano il fluorocromo legato al campione; 4) le radiazioni emesse dal fluorocromo (ad esempio in rosso) passano sia attraverso lo specchio dicroico (5) sia il filtro di sbarramento (6), il quale, invece, blocca le eventuali radiazioni non assorbite. Filtro di eccitazione 2 Filtro dicroico Obiettivo 3 4 Occhio Filtro di sbarramento 5 6 Lampada a vapori di mercurio 1
- 18. L’IMMUNOFLUORESCENZA L’immunofluorescenza permette la visualizzazione di antigeni mediante anticorpi precedentemente marcati con fluorocromi. Con la marcatura, all’anticorpo viene legato un fluoro- cromo, quindi l’anticorpo marcato reagendo con l’anti- gene specifico, lo renderà visibile in fluorescenza. ANTIGENE ANTICORPO Complesso AG/AC ANTIGENE ANTICORPO MARCATO Complesso AG/AC MARCATO
- 19. Il MICROSCOPIO CONFOCALE focalizza selettivamente un piano per volta nello spessore dell’oggetto e poi ricostruisce elettronicamente l’immagine finale mettendo insieme tutte le altre
- 20. Microscopio elettronico a trasmissione Nel microscopio elettronico a trasmissione gli elettroni generati da un tubo catodico, sotto vuoto spinto, vengono convogliati da un primo campo (condensatore) sul campione. Gli elettroni che lo attraversano vengono raccolti da un secondo campo magnetico (obiettivo) e inviati ad un campo magnetico (proiettivo) ed infine proiettati su una schermo fluorescente e/o su una lastra fotografica, dove si possono osservare zone chiare, corrispondenti a parti del campione attraversate dagli elettroni ( zone elettron-chiare) e zone scure, corrispondenti a zone opache agli elettroni (zone elettron-dense). La degli elettroni è in relazione con la differenza di potenziale applicata al tubo catodico secondo la formula: Tubo catodico 1°Campo magnetico Fascio di elettroni Campione 2°Campo magnetico Schermo fluorescente e lastra fotografica 3°Campo magnetico Se V = 100.000, sarà circa 0.04 nm. Applicando la formula di ABBE (P.R.= /2n sen ), con una apertura numerica teorica prossima a 1, il potere di risoluzione del microscopio elettronico sarebbe di P.R. (teorico) 0,02 nm. In pratica, a causa delle distorsioni causate dai campi magnetici, il P.R. (effettivo) è di 0,2 nm. 15 = V √
- 21. Microscopo elettronico a scansione - SEM
- 22. Microscopio elettronico a scansione Elaboratore immagini E’ principalmente impiegato per lo studio topografico della superficie dei campioni in esame. Tale microscopio utilizza un sottile raggio di elettroni primari (circa 7 nm) che tramite l’unità di scansione esplora il campione, in precedenza fissato e rivestito da un sottile strato di metalli pesanti (oro, oro-palladio). La superficie del campione eccitata dal fascio di elettroni primari emette elettroni secondari (e Raggi X), i quali tramite il rilevatore raggiungono l’elaboratore di immagine. L’unità di scansione sincronizza la scansione sul campione e sul monitor dell’elaboratore; pertanto l’immagine finale riproduce la struttura della superficie esplorata con effetto tridimensionale ad una risoluzione di solito di 20 nm.
- 23. Problematiche per l’osservazione dei preparati biologici L’osservazione al microscopio ottico o elettronico dei campioni biologici richiede che i preparati siano sufficientemente sottili da risultare trasparenti al fascio di luce o di elettroni e che sia preservata la morfologia delle cellule e degli organelli in esse contenuti.
- 25. Tecnica delle fette : prelievo e fissazione Chimica Coagulanti 2-FISSAZIONE Fisica Congelamento- Sostituzione Congelamento- Essiccazione Congelamento Alcool etilico Alcool metilico Sublimato corrosivo Acido picrico Acido acetico Alcool tricloracetico Non coagulanti Formalina Tetrossido di osmio (Ha lo scopo di bloccare la lisi delle cellule e dei tessuti e di preservarne il più possibile la struttura) 1- Prelievo Il prelievo dell’organo, solitamente di dimensioni al di sotto del cm 3 , va eseguito rapidamente, e se necessario, iniettando il fissativo con perfusione
- 26. Tecnica delle fette: fissazione e disidratazione Fissa-tivo 1-24 ore 5 - Chiarificazione in solventi organici (xilene – Histolemon) 2-Fissazione Histolemon I 1-24 ore 1-24 ore 4 - Disidratazione – serie ascendente degli alcol 100° II 50° 75° 95° 100° I Alcol Alcol Alcol Alcol Alcol 1-24 ore 1-24 ore 1-24 ore 1-24 ore 1-24 ore Acqua o tamponi 1-24 ore 3-Lavaggio Histolemon II 1-Prelievo organo
- 27. Tecnica delle fette: inclusione in paraffina 6 - Inclusione in paraffina viene effettuata in paraffina liquida, mantenuta a 60°C in apposite stufe, dove, preferibilmente, è possibile effettuare il vuoto. Blocchetti pronti per il taglio al microtomo Preparazione blocchetti - Il campione è immerso paraffina liquida, contenuta in contenitori prestampati o in lamelle di rame. La paraffina è poi lasciata solidificare a temperatura ambiente per 24 ore Lamelle di rame
- 28. Tecnica delle fette: sezioni al microtomo Microtomo rotativo Microtomo Leica - semiautomatico RM 2245 7-Sezioni al microtomo Il Microtomo – è uno strumento che permette di ottenere fette del campione incluso in paraffina dello spessore di 3-10 mm 8-Distensione delle fette su vetrini – si ottiene mettendo le fette sulla superficie dell’acqua portata ad una temperatura tra i 40-50 °C
- 29. Tecnica delle fette: colorazione e montaggio in balsamo 9-Sparaffinatura in solventi organici - elimina la paraffina dalle fette 10- serie discendente degli alcool e idratazione – viene effettuata gradualmente tramite passaggi in alcol a gradazione decrescente 11-Colorazione – può essere dicromica (emallume -eosina) o tricromica (ad esempio tricromica di Mallory) 12-Disidratazione – si effettuta tramite il passaggio dei vetrini nella serie ascendente degli alcool. 13-Chiarificazione – si effettuata tramite il passaggio in solventi organici 14-Monta g gio in balsamo – consiste nell’interporre una resine sintetiche tra vetrino porta- e coprioggetti) Colorazione dicromica (Emallume eosina) Colorazione tricromica di Mallory http://www.scienzebiologiche.unina.it/Download/Esercitazioni_Odi_Angi_Gua.pdf
- 31. Schema della Tecnica delle fette in Microscopia elettronica Preparazione dei campioni per l’osservazione in microscopia elettronica
- 32. Confronto tecniche delle fette in Microscopia ottica ed elettronica inclusione sezionamento spessore fette supporto colorazione montaggio Passaggio fissazione Microscopia ottica formalina+ac.picrico paraffina microtomo 7 - 10 µm vetrino coloranti organici balsamo Microscopia elettronica glutaraldeide, ac.osmico resine epossidiche ultramicrotomo 80-100 nm retino di rame metalli pesanti si butta
- 33. Particolari tecniche in uso in microscopia elettronica Colorazione negativa – viene applicata soprattutto per lo studio dei virus e delle macromolecole*. Il campione, sospeso in un colorante elettrondenso, è applicato su un retino ricoperto da un sottile film di plastica. Si asciuga all’aria e si osserva al TEM. Il colorante riempie gli spazi vuoti, che appariranno scuri, mentre i virus o le macromoleche risultano chiari Batteriofago evidenziato tramite colorazione negativa
- 34. Particolari tecniche in uso in microscopia elettronica- II Ombreggiatura al platino – è usato per lo studio delle macromolecole. 1) Il campione è adsorbito su un supporto liscio (lastra di mica). 2) Sotto vuoto spinto e sotto rotazione, sul campione viene proiettato, sotto un angolo di 5°-15°, un sottile strato di platino (elettron-denso) che evapora da un elettrodo al Platino reso incandescente. 3) Lo strato di platino, che rappresenta + + Pt C 1 2 3 4 5 6 la replica della superficie del campione, è stabilizzato da uno strato di carbone fatto cadere dall’alto da un elettrodo di carbone (elettron-chiaro). 4) la replica di platino è prima trasferita in un bagno alcalino che degrada il campione e, quindi, dopo lavaggio, (5) è trasferita su un retino per l’osservazione al TEM(6) Molecole di miosina Ombreggiate al platino
- 35. Particolari tecniche in uso in microscopia elettronica- II Senza crioprotezione, sotto vuoto spinto l’acqua contenuta nello strato superficiale del campione evapora. Ciò consente che membrana di un globulo rosso – osservata al TEM dopo criofrattura e ombreggiatura al platino– Il freeze etching è tecnica particolarmente usata per lo studio della struttura interna delle membrane cellulari e delle strutture cellulari interne. Il campione, opportunamente crioprotetto (1), è immerso in azoto liquido (2); in tal modo l’acqua vetrifica. Il campione è immesso sotto vuoto e quindi è inciso da una lama (3). Il piano di frattura prezerenzialmente avviene lungo il doppio strato delle mambrane biologiche (4). La superficie esposta dalla frattura è poi ombreggiata al platino (5) e rinforzata da una strato di carbone. La sostanza organica del campione viene rimossa mediante digestione alcalina e la replica metallica dopo lavaggio è osservata al microscopio elettronico(6). la criofrattura avvenga in uno strato cellulare più interno Nella foto si osserva una microvescicola legata ad un microtubulo. 1 2 3 4 5 6
- 36. Particolari tecniche – metodo di purificazione degli organelli cellulari Omogeneizzatore. Opera la dissociazione cellulare lasciando integri i nulcei e gli organelli cellulari. La sospensione cellulare ottenuta è sottoposta a centrifugazione differenziale Centrifugazione a 1.000 g per 10 minuti- sedimentano i nuclei . . . . . . . . . Centrifugazione a 10.000 g per 20 minuti- sedimentano i mitocondri Centrifugazione a 100.000 g per 60 minuti- sedimentano le vescicole microsomiali Centrifugazione a 160.000 g per 60 minuti- sedimentano i ribosomi o o o o o o o o o o o o o o o o o o o o o o o o . . . . . . . . o o o o o o o o o o o o o o o o o o o o o o o o o o o o . . . . . . . . . . . . . . . o o o o o o o o o o o o o o o o o o . . . . . . . . .